下列说法正确的是
①CH3COONa、BaSO4都是强电解质; ②中和滴定过程中,应注视锥形瓶内溶液颜色的变化,以准确把握滴定终点; ③测定溶液的PH值时,用玻璃棒蘸取少量溶液点在湿润的pH试纸上再与标准比色卡对照; ④ 0.1 mol·L-1 NaOH溶液与0.1 mol·L-1 Ba(OH)2溶液的PH相同; ⑤日用铝制品表面覆盖着氧化膜,对内部金属起保护作用。
| A.①②④ | B.①②⑤ | C.②③⑤ | D.③④⑤ |
下列物质中,不能发生消去反应的是()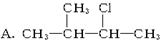 B. CH2 CH2Br2
B. CH2 CH2Br2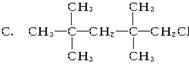 D.CH2ClCH2CH3
D.CH2ClCH2CH3
有机物 能发生的反应有( )
能发生的反应有( )
①取代反应 ②加成反应 ③ 消去反应 ④ 使溴的四氯化碳溶液褪色
⑤ 聚合反应 ⑥ 使酸性高锰酸钾溶液褪色
| A.全部 | B.除⑤外 | C.除①外 | D.除①、⑤外 |
将0.1mol两种气态烃组成的混合气体完全燃烧后得3.36L(标准状况)CO2和3.6gH2O下列说法正确的是
| A.一定有乙烯 | B.一定有甲烷 | C.可能有丙烯 | D.可能有乙烷 |
下列有机化合物有顺反异构体的是()
| A.CH3CH3 | B.CH2=CH2 | C.CH3CH=CH2 | D.CH3CH=CHCH3 |
实验室制硝基苯时,正确的操作顺序应该是 ( )
| A.先加入浓硫酸,再滴加苯,最后滴加浓硝酸 |
| B.先加入苯,再加浓硝酸,最后滴入浓硫酸 |
| C.先加入浓硝酸,再加入苯,最后加入浓硫酸 |
| D.先加入浓硝酸,再加入浓硫酸,最后滴入苯 |