向1LFeBr2溶液中,通入1.12L(标态下)的Cl2,测得溶液中c(Br-)=3c(Cl-),反应过程中溶液的体积变化不计,则下列说法中正确的是
| A.原溶液的浓度为0.1mol/L | B.反应后溶液中c(Fe3+)=0.1mol/L |
| C.反应后溶液中c(Fe3+)=c(Fe2+) | D.原溶液中c(Br-)=0.4mol/L |
有机化合物A(C8H8O2)为一种无色液体。从A出发可发生如图的一系列反应。则下列说法正确的是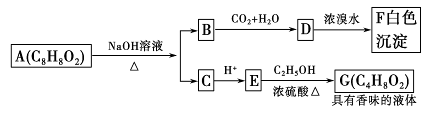
A.根据图示可推知D为苯酚
B.G的同分异构体中属于酯且能发生银镜反应的只有一种
C.上述各物质中能发生水解反应的有A、B、D、G
D.A的结构中含有碳碳双键
普罗加比对癫痫、痉挛和运动失调均有良好的治疗效果,其结构如图所示,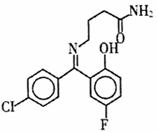
有关普罗加比的说法正确的是
| A.该分子在1H核磁共振谱中有12个峰 |
| B.一定条件下,1 mol普罗加比最多能与2 mol H2发生加成反应 |
| C.久置在空气中的普罗加比会因氧化而变质 |
| D.普罗加比可以和NaOH溶液、Na2CO3溶液反应,也可以和盐酸反应 |
下列说法不正确的是
| A.在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH |
| B.用甘氨酸和丙氨酸缩合最多可形成4种二肽 |
| C.分子式为C4H6O2,既能与NaOH溶液反应又能与溴的四氯化碳溶液反应的有机物有4种 |
D.乳酸薄荷醇酯( )能发生水解、氧化、消去反应 )能发生水解、氧化、消去反应 |
下列实验装置图正确且能达到实验目的的是
下列有关工程塑料PBT( )的说法中,正确的是
)的说法中,正确的是
| A.PBT是通过缩聚反应得到的高分子化合物 |
| B.PBT分子中含有羧基、羟基和酯基 |
| C.PBT的单体中有芳香烃 |
| D.PBT的单体均能与Na、NaOH、Na2CO3反应 |