某学生做浓度对化学反应速率的影响实验时,将3支试管编号为①②③,并按下表中的物质的量进行实验,记录的时间数据是16s、28s、33s。请将3个时间数据填入下表的适当位置,并写出实验结论。
| 试管编号 |
加3%Na2S2O3溶液/ml |
加H2O/ml |
加H2SO4(1:5)/滴 |
出现浑浊所用时间/s |
| ① |
3[ |
3 |
5 |
a |
| ② |
4 |
2 |
5[] |
b |
| ③ |
5 |
1 |
5 |
c |
(1) a= 、b= 、 c=
(2)实验结论:
(3)写出反应的化学方程式:  [来源:
[来源:
下图是某化学兴趣小组设计的乙醇催化氧化的实验装置(图中加热仪器.铁架台.试管夹均未画出)。图中A处为无水乙醇(沸点78℃),B处为绕成螺旋状的细铜丝,C处为无水CuSO4粉末,D处为碱石灰,F处为新制的碱性Cu(OH)2悬浊液。
(1)在上述装置中,实验需要加热的仪器按加热的先后顺序排列为(填序号)。
(2)为使A中乙醇平稳地汽化成乙醇蒸气,常用的方法是。
(3)写出B处的现象。
某同学为了验证海带中含有碘,拟进行以下实验,请回答相关问题。
(1)第1步:灼烧。操作时将足量海带灼烧成灰烬,该过程中将使用到的硅酸盐质实验仪器有(填代号,限填3项)
A.试管 B.瓷坩埚 C.坩埚钳 D.三脚架
E.泥三角 F.酒精灯 G.烧杯 H.量筒
(2)第2步:I-溶液的获取。操作是。
(3)第3步:氧化的操作中依次加入合适的试剂。下列氧化剂最好选用(填代号)
A.浓硫酸 B.新制氯水 C.高锰酸钾溶液 D.双氧水
(4)第4步:碘单质的检验,操作是取少量第3步的溶液,滴加淀粉溶液,如果溶液显蓝色,则证明海带中含有碘。
某化学小组以苯甲酸为原料制取苯甲酸甲酯,并用制得的苯甲酸甲酯进行碱性水解的实验。
I.制取苯甲酸甲酯:已知有关物质的沸点如下表:
| 物质 |
甲醇 |
苯甲酸 |
苯甲酸甲酯 |
| 沸点/℃ |
64.7 |
249 |
199.6 |
实验装置如下:
(1)简述第一步混合液体时,最后加入浓硫酸的理由是
。
若反应产物水分子中有同位素18O,写出能表示反应前后18O位置的化学方程式:
。
(2)分液时上层液体从出来;接受馏分时温度控制在。
(3)此制取过程比教材中乙酸乙酯的制备复杂很多,写出用此过程制备苯甲酸甲酯的两大优点:、。
II、苯甲酸甲酯碱性水解

(4)写出苯甲酸甲酯碱性水解的化学反应方程式。
(5)写出苯甲酸甲酯碱性水解实验装置中A的作用。
III、苯甲酸甲酯有多种同分异构体
(6)符合下列条件的结构
①可以发生银镜反应②属于芳香族化合物③不具备其它环状结构④不能与FeCl3发生显色反应;共有种。
影响化学反应速率的因素很多,某课外兴趣小组用实验的方法通过图1所示装置研究反应速率的有关问题。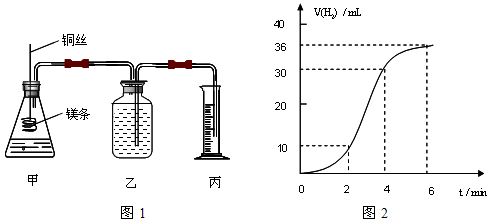
(1)取一段镁条,用砂纸擦去表面的氧化膜,使镁条浸入锥形瓶内的稀盐酸中。足量镁条与一定量盐酸反应生成H2的量与反应时间的关系曲线如图2所示。
①请在图3 的方框中画出上述反应的速率(mL/min)与时间(min)的关系曲线。
②在前4min内,镁条与盐酸的反应速率逐渐加快,在4min之后,反应速率逐渐减慢,请简述其原因:。
(2)某同学发现,纯度、质量、表面积都相同的两铝片与H+浓度相同的盐酸和硫酸在同温同压下反应时产生氢气的速率差别很大,铝和盐酸反应速率更快。他决定对其原因进行探究。填写下列空白:
①该同学认为:由于预先控制了反应的其他条件,那么,两次实验时反应的速率不一样的原因,只有以下五种可能:
原因Ⅰ:Cl-对反应具有促进作用,而SO42-对反应没有影响;
原因Ⅱ:_______________________________________________________;
原因Ⅲ:Cl-对反应具有促进作用,而SO42-对反应具有阻碍作用;
原因Ⅳ:Cl-、SO42-均对反应具有促进作用,但Cl-影响更大;
原因Ⅴ:________________________________________________________。
②该同学设计并进行了两组实验,即得出了正确结论。他取了两片等质量、外形和组成相同、表面经过砂纸充分打磨的铝片,分别放入到盛有同体积、c(H+)相同的稀硫酸和盐酸的试管(两试管的规格相同)中:
a.在盛有硫酸的试管中加入少量NaCl或KCl固体,观察反应速率是否变化;
b.在盛有盐酸的试管中加入少量Na2SO4或K2SO4固体,观察反应速率是否变化。
若观察到实验a中___________________,实验b中__________________________,则说明原因Ⅲ是正确的。依次类推。该同学通过分析实验现象,得出了结论:Cl-对反应具有加速作用。
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中;
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数;
③向锥形瓶中滴入酚酞作指示剂,进行滴定。滴定至终点,测得所耗盐酸的体积为V1mL;
④重复以上过程,但在滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL。
试回答下列问题:
(1)滴定终点时的现象为锥形瓶中的溶液由__________ _ _____。
(2)滴定时边滴边摇动锥形瓶,眼睛应观察_________________;
(3)该小组在步骤①中的错误是_____________ _ _______,由此造成的测定结果_________(填偏高、偏低或无影响);
(4)步骤②缺少的操作是_______ ____;
(5)下图,是某次滴定时的滴定管中的液面,其读数为___________mL;
(6)根据下列数据:
| 滴定次数 |
待测液体积(mL) |
标准盐酸体积(mL) |
|
| 滴定前读数(mL) |
滴定后读数(mL) |
||
| 第一次 |
25.00 |
0.40 |
20.38 |
| 第二次 |
25.00 |
4.00 |
24.02 |
请计算待测烧碱溶液的物质的量浓度。(请写出解答过程)