废旧塑料回收和利用是减轻“白色污染”、实现资源再利用的有效途径之一。某兴趣小组进行如下探究:
[实验课题]废旧聚丙烯塑料热分解主要产物的探究
[查阅资料]①石蜡热分解的产物为常温下的气态烃和液态烃
②CuO能将烃氧化成CO2和H2O
③苯甲酸能溶于苯
[实验设计][
[实验记录]
①B装置试管中有液态物质生成;②C中溴水的颜色变浅;③E装置中黑色氧化铜变红;④F装置中无水硫酸铜变蓝。
[问题讨论]请你参与实验设计的评价和实验结果的分析:
(1)经分析得知B装置试管 中的液态产物是甲苯和苯的混合物。若要除去其中的甲苯,
中的液态产物是甲苯和苯的混合物。若要除去其中的甲苯,
实验操作方法是
(2)C装置的作用是 ;
(3)如果不设置D装置,对实验结论产生的影响是
 。
。
(4)甲同学认为从C中出来的气体是氢气,乙同学认为还可能有其它成分。你认为其
他成分可能是 。为完善实验设计,请在上图方框内画出装置图并注明其中盛放的试剂名称。
(每空1分,共8分)实验室需要配制0.1 mol/L CuSO4溶液480 mL。按下列操作步骤填上适当的文字,以使整个操作完整。
(1)选择仪器。完成本实验所必需的仪器有:托盘天平(精确到0.1 g)、药匙、烧杯、玻璃棒、________、________以及等质量的两片滤纸。
(2)计算,应选择下列正确________
| A.需要CuSO4固体8.0g | B.需要CuSO4·5H2O晶体12.0 g |
| C.需要CuSO4·5H2O晶体12.5 g | D.需要CuSO4固体7.7 g |
(3)称量。所用砝码生锈则所配溶液的浓度会________(填“偏高”、“偏低”或“无影响”)。
(4)溶解、冷却,该步实验中需要使用玻璃棒,目的是_________________。
(5)转移、洗涤。在转移时应使用________引流,需要洗涤烧杯2~3次是为了___________________。
(6)定容,摇匀。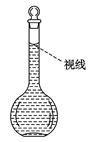
(7)将配好的溶液静置一段时间后,倒入指定的试剂瓶,贴好标签,注明配制的时间、溶液名称及浓度。
(8)在配制过程中,某学生观察定容时液面情况如图所示,所配溶液的浓度会________(填“偏高”、“偏低”或“无影响”)。
某化学兴趣小组采用下列方法测定Na2SO3样品中Na2SO4的质量分数。
【方法一】 测 SO2质量法采用如图所示装置,通过实验测定生成SO2的质量。
测 SO2质量法采用如图所示装置,通过实验测定生成SO2的质量。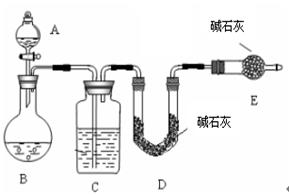
(1)C中盛放的试剂是,E装置的作用是。
(2)若实验前称取m1g样品,再测得SO2的质量为m2g,则可得Na2SO4质量分数,其中m2是通过
测定(填装置符号)装置在实验前后的质量差得到的。该方法的缺点是(只答一点)
。
【方法二】测沉淀质量法
第一步:称取m3g样品,置于小烧杯中第二步:向小烧杯中加入足量稀盐酸,加热
第三步:再向小烧杯中加入足量BaCl2溶液,然后过滤、洗涤第四步:干燥沉淀,称重为m4g
(3)方案中BaCl2能否改成Ba(NO3)2?(填“能”或“不能”); 试简述原因
。
(4)简述洗涤沉淀的方法:。
(5)若m3=2m4则试样中Na2SO4的质量分数为。
(12分) (1)高锰酸钾保存在棕色试剂瓶,下列试剂保存不需要棕色试剂瓶的是_______。
A.浓硝酸 B.硝酸银 C.氯水 D.纯碱
(2)下列实验中仪器的下端不能插入液面以下的是(填字母编号)。
A 蒸馏时用的温度计 B 制备乙烯时用的温度计
C 用水吸收氨气的导管口 D 用碱液吸收多余氯气的导管口
E.制备H2的简易装置中加入稀硫酸用的长颈漏斗
F.制备Fe(OH )2时,向FeSO4溶液中滴入NaOH溶液用的胶头滴管
(3)下列有关实验的叙述,正确的是(填字母编号)。
A用98%的浓硫酸配制100g10%的稀硫酸溶液时,除使用量筒外还需用到容量瓶
B测定溶液的pH时,可用洁净、干燥的玻璃棒蘸取溶液,滴在pH试纸上,再与标准比色卡比较
C不能用分液漏斗将乙醇和水的混合液体分离
D用浓氨水洗涤做过银镜反应的试管
E.用广泛pH试纸测得氯水的pH为2
F.用碱式滴定管量取20.00mL0.1000mol/L的高锰酸钾溶液
G.用托盘天平称取10.50g干燥的NaCl固体
H.配制一定物质的量浓度的溶液,定容时俯视容量瓶的刻度线,会使所配溶液的浓度偏低
I.用瓷坩埚高温熔融NaOH和Na2CO3的固体混合物
(4)“磨砂”是增加玻璃仪器密封性的一种处理工艺。在仪器A.试管 B.分液漏斗 C.带滴管的试剂瓶(滴瓶) D.集气瓶 E.酸式滴定管 F.碱式滴定管中,没有用到“磨砂”工艺处理的有________。
(填字母编号)。
(5))下列各图所示装置的气密性检查中,一定漏气的是(填字母编号)。 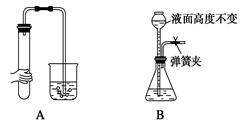
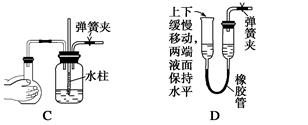
(6)下图各种尾气吸收装置中,适合于吸收NH3气体,而且能防止倒吸的有_____________。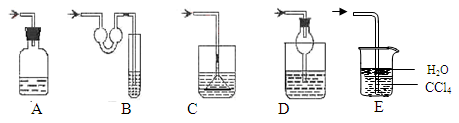
( 9 分)实验室里用乙醇和浓硫酸反应生成乙烯,乙烯再与澳反应制 1,2 一二溴乙烷。在制备过程中部分乙醇被浓硫酸氧化产生 CO2、SO2,并进而与B几反应生成HBr等酸性气体。
已知:CH3CH2OH CH2=CH2↑+ H2O
CH2=CH2↑+ H2O
(1)用下列仪器,以上述三种物质为原料制备 1,2 一二溴乙烷。如果气体流向为从左到右,正确的连接顺序是(短接口或橡皮管均已略去): B经A①插人A中, D接A②;A③接接接接。
(2)装置C的作用是。
(3)装置F中盛有10 % Na0H 溶液的作用是。
(4)在反应管E中进行的主要反应的化学方程式为。
(5)处理上述实验后三颈烧瓶中废液的正确方法是。
A.废液经冷却后倒人下水道中
B.废液经冷却后倒人空废液缸中
C.将水加人烧瓶中稀释后倒人空废液缸中
( 9分)重铬酸钾(K2Cr2O7)是重要氧化剂,重铬酸钾的溶解度受温度影响较大,工业上常用铬铁矿(主要成分为FeO•Cr2O3,杂质为SiO2•Al2O3)为原料生产它。实验室模拟工业上用铬铁矿制 K2CrO7的主要工艺流程如下图。涉及“碱熔”的主要反应为:
6 FeO•Cr2O3 + 24NaOH + 7KC1O3 = 12NaCrO4 + 3Fe2O3 + 7KCl + 12H2O
(1)使用粉末状铬铁矿的目的是。
(2)调节pH后,过滤得到的滤渣是(填化学式)。
(3)酸化Na2CrO4溶液时,其平衡转化的离子方程式为。
(4)称取重铬酸钾试样2.500g配成500mL溶液,取出25.00mL于锥形瓶中,加入10 mL2mol/LH2SO4和足量碘化钾(铬的还原产物为Cr3+),放于暗处5min。然后加入100 mL 水,加人3mL淀粉溶液(作指示剂),用0.1200 mol/LNa2S2O3标准溶液滴定( I2 + 2S2O2- 3= 2I-+S4O2- 6),用去20.00mL ,则该样品的纯度为。