某课外活动小组利用下图装置探究SO2与Na2O2的反应。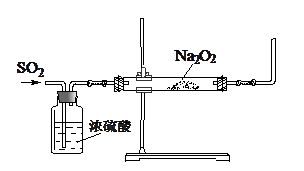
(1)请指出该装置中一个不合理的地方: 。
(2)第1小组同学认为Na2O2与SO2反应类似CO2与Na2O2的反应,该反应的化学方程式为 。
(3)第2小组同学认为Na2O2与SO2反应除了生成Na2SO3和O2外,还有Na2SO4生成。他们作出这个推断的理由是 。
(4)第3小组在通入过量SO2后,请你完成对反应完毕后硬质玻璃管中的固体成分的探究。
限选用的试剂:蒸馏水、稀盐酸、稀硫酸、稀硝酸、浓盐酸、浓硫酸、浓硝酸、Ba(NO3)2溶液、BaCl2溶液、1moL·L-1NaOH、0.01mol·L-1KMnO4、紫色石蕊试液。
①提出对玻璃管中固体成分的合理假设:
假设Ⅰ:全部为Na2SO3;
假设Ⅱ:为Na2SO3和Na2SO4的混合物;
假设Ⅲ: ;
②设计实验方案(不要在答题卡上作答)。
③实验过程
根据②的实验方案,请在答题卡上写出实验步骤以及预期现象和结论。
| 实验步骤 |
预期现象和结论 |
| 步骤1:用药匙取少量固体于试管中,加入适量蒸馏水充分溶解后,将所得溶液分置于A、B试管中。 |
|
| 步骤2: |
|
| 步骤3: |
|
某生用0.1000mol/L的KOH标准溶液滴定未知浓度盐酸,其操作可分解为如下几步:
| A.移取20.00mL待测盐酸溶液注入洁净的锥形瓶,并加入2~3滴酚酞 |
| B.用标准溶液润洗滴定管2~3次 |
| C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液 |
| D.取标准KOH溶液注入碱式滴定管至刻度0以上2~3cm |
E、调节液面至0或0以下刻度,记下读数
F、把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点并记下滴定液面的刻度。
就此实验完成填空:
(1)正确操作步骤的顺序是(用序号字母填写)。
(2)上述B步骤操作的目的是。
(3)上述A步骤操作之前,先用待测液润洗锥形瓶,则对滴定结果的影响是。
(4)判断到达滴定终点的实验现象是:。
(5)若称量一定量的KOH固体(含少量NaOH)配制标准溶液并用来滴定上述盐酸则对滴定结果的影响是。
工业上制取CuCl2的生产流程如下: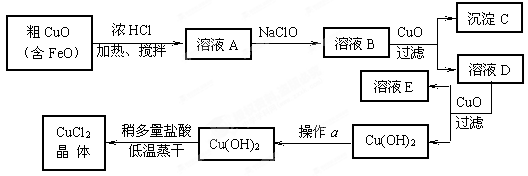
请结合下表数据,回答下列问题:
| 物质 |
Fe(OH)2 |
Cu(OH)2 |
Fe(OH)3 |
| 完全沉淀时的pH范围 |
≥9.6 |
≥6.4 |
3~4 |
⑴ 溶液A中加入NaClO的目的是;
此反应离子方程式为;
⑵ 在溶液B中加入CuO的作用是;
⑶ 操作a的目的是;
⑷ 在Cu(OH)2加入盐酸使Cu(OH)2转变为CuCl2。采用多量盐酸和低温蒸干的目的是。
某学生为测定未知浓度的硫酸溶液,以0.1400mol/L的NaOH溶液滴定上述H2SO4,取待测硫酸25.00mL,滴定终止时消耗NaOH溶液15.00mL。
(1)若使用甲基橙做指示剂,如何确定终点 (2)下列操作将导致测定值高于实际值的是
| A.标准液在“0”刻度线以上,未予调整就开始滴定 |
| B.碱式滴定管用蒸馏水洗涤后未用标准NaOH溶液润洗 |
| C.观察记录滴定管内液面刻度时滴定前仰视,滴定后俯视 |
| D.酸滴定管经蒸馏水洗净后,即注入锥形瓶进行中和滴定 |
E.在滴定过程中不慎将数滴酸液滴在锥形瓶外
(3)计算待测硫酸溶液的物质的量浓度为 mol/L(计算出结果到小数点后二位)
某同学设计了一个简单的实验(如图所示),以测定镁铝合金中铝的质量分数。可供选用的试剂有:浓H2SO4、浓硝酸、6 mol·L-1 NaOH溶液。
请填写下列空白:
(1)有关实验操作:a、往试管中放入适量的铝合金样品;b、从分液漏斗往试管中加入过量的A溶液;c、检查装置的气密性;d、测定收集到的水的体积。
正确的操作顺序为_______________________________(填字母)。
(2)A溶液可选用___________________________________________
(3)写出实验中发生反应的化学方程式:_________________________________________。
(4)若实验中测得样品的质量为Wg ,氢气的体积为a L(标准状况),则样品中Al的质量分数为___。
在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应。应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”。请回答该实验中的问题。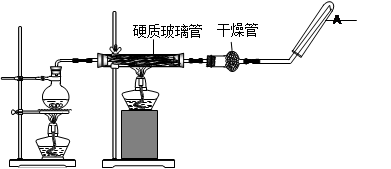
(1)写出该反应的反应方程式;并指明该氧化还原反应的还原剂是(填化学式,下同),氧化剂是。
(2)圆底烧瓶中盛装的水,该装置受热后的主要作用是;烧瓶底部放置了几片碎瓷片,其作用是 。
(3)试管中收集气体是(填化学式),如果要在A处玻璃管处点燃该气体,则必须对该气体进行。
(4)该同学欲确定反应后硬质试管中还原铁粉是否完全反应,其中的固体成分有哪些,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红色则说明硬质试管中固体物质一定有,若溶液未变红色则说明硬质试管中固体物质的成分是。
(5)该同学按上述实验方案进行了实验,结果溶液未变红色,原因是(用离子方程式表示)。