已知:
1.冠心平是降血脂、降胆固醇的药物,它的一条合成路线如下

(1)为一元羧酸,8.8 与足量溶液反应生成2.24(标准状况),的分子式为。
(2)写出符合分子式的所有甲酸酯的结构简式:
。
(3)是氯代羧酸,其核磁共振氢谱有两个峰,写出的反应方程式:。
(4)的反应类型为。
(5)写出和的结构简式:
_; 。
(6)的苯环上有两种氢,它所含官能团的名称为;写出所代表的试剂:; 。
Ⅱ.按如下路线,由可合成高聚物:

(7)的反应类型为.
(8)写出的反应方程式:_。
24.5gH2SO4的物质的量是,1.5molNa2CO3的质量是。
解释钠投入滴有酚酞试液的水中,产生下列现象的原因:
(1)钠浮在水面
(2)钠熔化成闪亮的小球
(3) 钠小球在水面四处游动,并发出“嘶嘶”声
钠小球在水面四处游动,并发出“嘶嘶”声
(4)滴有酚酞试液的水变红
在高温时,水蒸气与灼热的炭发生氧化还原反应的化学方程式是H2O+C H2+CO,其中水是剂。硫在氧气中燃烧的化学方程式是,其中硫是剂。
H2+CO,其中水是剂。硫在氧气中燃烧的化学方程式是,其中硫是剂。
在某有机物A,其结构简式如图。请写出以下化学反应的方程式。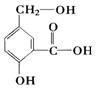
①A跟NaOH溶液反应:。
②A跟NaHCO3溶液反应:。
③A在一定条件下跟Na反应:。
(10分)已知:2CH2=CH2+O2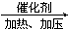 2CH3CHO,以乙烯、空气、水为原料在一定条件下能实现如下图所示的转化。
2CH3CHO,以乙烯、空气、水为原料在一定条件下能实现如下图所示的转化。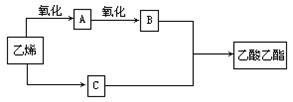
(1)物质C俗称_________,其结构简式为____________ ;
(2)写出由A→B的化学方程式____________________________;
(3)写出由B+C→乙酸乙酯的化学方程式____________________该反应是___________反应。