(1 3分)实验室用大理石等原料制取安全无毒的杀菌剂过氧化钙。大理石的主要杂质是氧化铁,以下是提纯大理石的实验步骤:
3分)实验室用大理石等原料制取安全无毒的杀菌剂过氧化钙。大理石的主要杂质是氧化铁,以下是提纯大理石的实验步骤:

(1)溶解大理石时,用硝酸而不同硫酸的原因是 _____________ 。
(2)操作Ⅱ的目的是 ____ ,溶液A(溶质是共价化合物)是 。
(3)写出检验滤液B中是否含NH4+离子方法: _______
_________________________________________________________________________
(4)写出加入碳酸铵所发生反应的离子方程式: _______ 。写出滤液B的一种用途: 。
X、Y、Z、W是常见的四种短周期元素,其原子序数依次增大。其相关信息如下表:
| 元素 |
相关信息 |
| X |
X的基态原子最外层电子排布式为nsnnpn |
| Y |
Y是空气中含量最高的元素 |
| Z |
Z是地壳中含量最高的金属元素 |
| W |
W的单质是常见的半导体材料 |
(1)Y位于元素周期表的 周期 族,Y与W的气态氢化物较稳定的是(写化学式)
(2)Z的单质与W的单质相比熔点较高的是(写化学式);Z与W原子半径较大的是 (写化学式)
(3)X的一种氧化物XO2分子中σ键与∏键数目之比为
(4)X的第一电离能比W的(填“大”或“小”)
(5)写出X的单质与Y的最高价氧化物水化物的浓溶液在加热的条件下反应的化学方程式:
(6)已知2.7gZ单质与足量Y单质反应,放出31.8kJ的热量,请写出此反应的热化学方程式:。
锗及其某些化合物是导弹火箭制导中的重要光电材料,工业上生产锗的流程如下: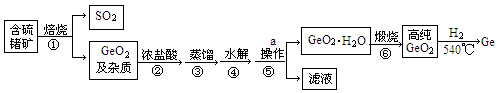
已知:GeO2与浓盐酸反应生成四氯化锗(熔点为—51.5℃,沸点为86.6℃)。四氯化锗易水解。
(1)步骤②中浓盐酸除了作为反应物外,还有一个重要作用是。
(2)步骤③控制的温度范围。
(3)写出反应的④、⑥的化学方程式
④;⑥。
(4)生产过程中可以循环利用的物质是(填化学式)
(5)步骤①中产生的SO2可以用碱液吸收,请写出离子反应方程式。
(6)请简要描述实验室中操作a的过程。
Favorskii反应是化工生产中的重要反应,它是利用炔烃与羰基化合物在强碱性下发生反应,得到炔醇,反应原理为: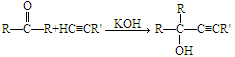
已知:
以下合成路线是某化工厂生产流程的一部分:
请回答下列问题:
(1)写出F中官能团的名称。
(2)写出D的名称(系统命名)。
(3)④的反应类型是;B的结构简式是。
(4)写出反应⑥的化学方程式为。
(5)H是D的同分异构体,核磁共振氢谱有3种峰且属于炔烃的结构简式为
、。
(6)有关C的说法正确的是
| A.能使溴的四氯化碳溶液褪色 | B.能和氢氧化钠溶液反应 |
| C.能使酸性高锰酸钾褪色 | D.能与乙酸发生酯化反应 |
X、Y、Z、W是元素周期表前四周期中的常见元素。其相关信息如下表:
| 元素 |
相关信息 |
| X |
X的一种核素的质量数为18,中子数为10 |
| Y |
Y与X同主族,且它的一种氧化物是导致酸雨的主要物质之一 |
| Z |
Z的单质常温下为黄绿色气体 |
| W |
W的基态原子核外有4个未成对电子 |
(1)Z位于元素周期表的位置,写出Z的原子结构示意图。
(2)Y的电负性比Z 的(填“大“或”小”);X和Y的气态氢化物中,较稳定的是(写化学式)。
(3)X的一种氢化物H2X2分子中极性键和非极性健数目之比为。
(4)Z的一种单质与烧碱溶液作用可以生产日常生活用的消毒剂,请写出其反应的离子方程式:。
(5)已知28gW在氧气中燃烧,放出186.4kJ的热量,请写出此反应的热化学方程式:。
短周期元素Q、R、T、W在元素周期表中的位置如右图所示,其中T所处的周期序数与主族序数相等,请回答下列问题: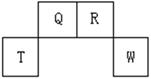
(1)W在周期表中的位置是, Q、R、T三种元素原子的半径从大到小排列顺序(用元素符号表示),Q的最高价氧化物的电子式,R气态氢化物分子的结构式为;
(2)元素的原子得电子能力:QW(填“强于”或“弱于”);
(3)原子序数比R多8的元素形成的一种常见气态氢化物的沸点(填“高”或“低”)于R的的常见气态氢化物;
(4)T、Q、R、W的单质中,固态时属于原子晶体的是(填名称);
(5)现有8种元素的性质、数据如下表所列,它们属于短周期:请指出R元素在下表中的对应编号,与T同周期且最高价氧化物的水化物碱性最强的元素在下表中的对应编号。
| ① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
|
| 原子半径(10-10m) |
0.74 |
1.60 |
1.52 |
1.10 |
0.99 |
1.6 |
0.75 |
0.82 |
| 最高或最低化合价 |
+2 |
+1 |
+5 |
+7 |
+1 |
+5 |
+3 |
|
| -2 |
-3 |
-1 |
-3 |