已知由三种元素构成的四种物质存在下列反应,其中a的分子空间构型为正四面体。组成a分子的两种元素的原子序数和小于10,组成b分子的元素为第三周期的元素。则下列判断正确的是
| A.四种分子中的化学键均是极性键 | B.a、c分子中中心原子均为sp3杂化 |
| C.四种分子中既有σ键,又有π键 | D.b、d分子中共价键的键能b大于d |
工业合成氨反应为3H2(g) + N2(g) ⇋2NH3(g) ΔH<0,下列措施能使反应物中活化分子百分数增大的方法是
①增大N2的浓度;②升高温度;③增大压强;④移去NH3;⑤加入催化剂;
| A.①②③ | B.①②③⑤ | C.①②③④⑤ | D.②⑤ |
一定温度下,反应N2+O2 2NO在密闭容器中进行,下列措施不改变化学反应速率的是
2NO在密闭容器中进行,下列措施不改变化学反应速率的是
| A.缩小体积使压强增大 | B.恒容,充入N2 |
| C.恒容,充入He | D.恒压,充入He |
四位同学同时进行反应:A(g)+3B(g)=2C(g)+2D(g) 的速率测定实验,分别测得反应速率如下:①v(A)=0.15mol/(L·s) ②v(B)= 0.6mol/(L·s) ③v(C)= 0.5mol/(L·min) ④v(D)= 0.45mol/(L·s)。其中,反应进行得最快的是
A.①B.② C.③D.④
反应2SO2(g)+O2(g)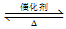 2SO3(g)经一段时间后,SO3的浓度增加了0.4 mol·L-1,在这段时间内用O2表示的反应速率为0.04 mol·L-1·s-1,则这段时间为
2SO3(g)经一段时间后,SO3的浓度增加了0.4 mol·L-1,在这段时间内用O2表示的反应速率为0.04 mol·L-1·s-1,则这段时间为
| A.0.1 s | B.2.5 s | C.5 s | D.10 s |
少量铁粉与100ml0.01mol/L稀盐酸反应。为了加快速率而不改变H2产量,可以使用如下方法中的:①加H2O ②加NaOH固体 ③滴入几滴浓盐酸 ④加NaCl溶液 ⑤滴加几滴硫酸铜溶液 ⑥适当升高温度(不考虑盐酸挥发) ⑦改用10ml 0.1mol/L的盐酸
| A.③⑤⑥⑦ | B.③⑥⑦ | C.③④⑤⑥⑦ | D.①③⑤⑦ |