(1)有人研究证明:使用氯气作自来水消毒剂,氯气会与水中有机物反应,生成如CHCl3等物质,这些物质可能是潜在的致癌致畸物质。目前人们已研发多种饮用水的新型消毒剂。下列物质不能作自来水消毒剂的是 (填序号)。
| A.硫酸铜 | B.二氧化氯 | C.臭氧 | D.硫酸亚铁 |
(2)高铁(VI)酸盐(如Na2FeO4)是新一代水处理剂。其制备方法有:次氯酸盐氧化法(湿法)和高温过氧化物法(干法)等。湿法是在碱性溶液中用次氯酸盐氧化铁(III)盐,写出该法的离子方程式:
。
(3)用高铁(VI)酸盐设计的高铁(VI)电池是一种新型可充电电池,电解质溶液为KOH溶液,放电时的总反应:3Zn+2K2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4KOH
①写出正极发生的电极反应式: 。
②用高铁(VI)电池作电源,以Fe作阳极,以Cu作阴极,对足量KOH溶液进行电解,当电池中有0.2molK2FeO4反应时,则在电解池中生成H2 L(标准状况)。
③下表列出了某厂排放的含锌废水中的含量及国家环保标准值的有关数据:
| |
某厂含锌废水水质 |
国家环保标准值 |
| Zn2+浓度/(mg·L-1) |
≤800 |
≤3.9 |
| pH |
1~5 |
6~9 |
该厂只用调节pH处理废水,当调整为pH=7时,此时废水中Zn2+的浓度为 mg/L, (填“符合”或“不符合”)国家环保标准。(常温下,Ksp[Zn(OH)2]=1.2×10-17)
现有:
| A.(CH3)3CCH2OH; | B.(CH3)3COH; | C.(CH3)2CHOH; | D.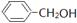 四种有机物 四种有机物 |
(1)能氧化成醛的是;
(2)能消去成烯的是;
(3)D与甲酸发生酯化反应的产物是。
下列各组中,属于同分异构体的是______;肯定属于同系物的是______; (填编号)
①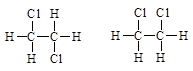
②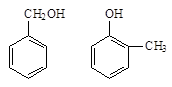
③C3H6与C4H8
④CH3OH与C5H11OH
请同学们根据官能团的不同对下列有机物进行分类。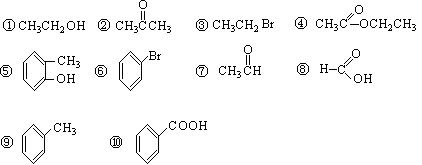
(1)芳香烃:; (2)卤代烃:;
(3)醇:;(4)醛:;
(5)羧酸:;(6)酯:。
Ⅰ.化合物甲、乙、丙有如下转化关系:
甲(C4H10O)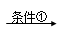 乙(C4H8)
乙(C4H8)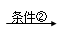 丙(C4H8Br2)
丙(C4H8Br2)
回答:
(1)甲中官能团的名称是________,甲可能结构有________种,其中可催化氧化为醛的有________种;使酸性KMnO4溶液褪色的有________种。
(2)甲→乙的反应类型为________,乙→丙的反应类型为________
Ⅱ.(1)乙醇、乙二醇、丙三醇中分别加入足量金属钠,产生等体积的氢气(相同条件下),则上述三种醇的物质的量之比是________。
(2)等质量的①甲醇 ②乙醇③乙二醇④丙三醇,分别和足量的金属钠作用,放出氢气的量由少到多的顺序是__________。(填序号)
含苯酚的工业废水的处理流程如图所示。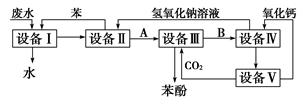
(1)①流程图设备Ⅰ中进行的是______操作(填写操作名称)。
②图中,能循环使用的物质是:C6H6、CO2______、______。
(2)为了防止水源污染,用简单而又现象明显的方法检验某工厂排放的污水中有无苯酚,此方法是_______________________________________________________。
(3)从废水中回收苯酚的方法是:①用有机溶剂萃取废液中的苯酚;②加入某种药品的水溶液使苯酚与有机溶剂脱离;③通入某物质又析出苯酚。试写出②、③两步的反应方程式:
_________________________________________________________________________________________。