(共10分)下表是A、B、C、D、E五种有机物的有关信息:
| A |
①能使溴的四氯化碳溶液褪色 ②比例模型如图 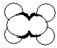 ③能与水在一定条件下反应生成C |
| B |
①由C、H两种元素组成 ②球棍模型如图 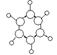 |
| C |
①由C、H、O三种元素组成 ②能与Na反应 ③与E反应生成相对分子质量为88的酯 |
| D |
①相对分子质量比C少2 ②能由C催化氧化得到 |
| E |
①由C、H、O三种元素组成 ②其水溶液能使紫色石蕊试液变红 |
回答下列问题:
(1)A~E中,属于烃的是__________(填字母)。
(2)A能使溴的四氯化碳溶液褪色,发生反应的化学方程式为_______________________。
(3)C催化氧化生成D的化学方程式为________________________。
(4)有机物B具有的性质是_____________(填序号)。
①无色无味的溶液;②有毒;③不溶于水;④密度比水大;
⑤能使酸性KMnO4溶液和溴水褪色。
(5)E的水溶液能使紫色石蕊试液变红,说明E的水溶液显酸性,现设计一个实验来比较E与碳酸酸性的强弱,则该实验的原理是_____________________________(用化学方程式说明)。
在如图所示的装置中,若通入直流电5min时,铜电极质量增加2.16 g,试回答:
(1) 电源电极X为________极。
(2) pH变化:A________,B________,C________。(填“增大”、“减小”或“不变”)
(3) 通电5 min时,B中共收集224 mL气体(标准状况),溶液体积为200 mL。则通电前CuSO4溶液的物质的量浓度为________(设电解前后溶液体积无变化)。
(4) 若A中KCl溶液的体积也是200 mL,电解后,溶液的pH为________(设电解前后溶液体积无变化)。
(1)体积相同、浓度均为0.2mol/L的盐酸和醋酸溶液分别加水稀释10倍,溶液的pH分别变成m和n,则m和n的关系是________,稀释后两溶液中和NaOH的能力_______。
(2)25℃时,pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合,混合后溶液呈_____(填“酸性”“碱性”或“中性”),混合后溶液中离子浓度由大到小的顺序是_______________________。
(3)25℃时,将VamLpH=1的硫酸溶液与VbmLpH=12的氢氧化钾溶液混合恰好呈中性,则Va:Vb=________。
、对于弱酸,在一定温度下达到电离平衡时,各微粒的浓度存在一种定量的关系。若25℃时有HA H++A―,则K=
H++A―,则K= 。式中:K为电离平衡常数,只与温度有关,c为各微粒的平衡浓度。下表是几种常见弱酸的电离平衡常数(25℃)。
。式中:K为电离平衡常数,只与温度有关,c为各微粒的平衡浓度。下表是几种常见弱酸的电离平衡常数(25℃)。
回答下列问题:
(1)当升高温度时,K值____(填“变大”“变小”或“不变”)。
(2)在温度相同时,各弱酸的K值不同,那么K值的大小与酸性的相对强弱有何关系?____ ________。
(3)若把CH3COOH、H2CO3、HCO3-、H2S、HS-、H3PO4、
H2PO4-、HPO42-都看做是酸,其中酸性最强的是_,最弱的是_ __。
(4)同一多元弱酸的K1、K2、K3之间存在着数量上的规律,此规律是_____________,产生此规律的原因是_____________ ___。
(5) Na2CO3溶液呈_ _(填“酸性”“碱性”或“中性”),其原因(用离子方程式表示)是_。
(6)已知NaH2PO4溶液呈酸性,则该溶液中c(H3PO4)____c(HPO42-)(填“大于”或“小于” )。
(16分) 接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:2SO2(g)+O2(g) 2SO3(g)ΔH=-190kJ·mol-1
2SO3(g)ΔH=-190kJ·mol-1
(1)该热化学反应方程式的意义是_______________________________________________
升高温度上述反应平衡常数____(填“变大”“变小”或“不变”)。
(2)下列描述中能说明上述反应已达平衡的是________。
a.v(O2)正=2v(SO3)逆
b.容器中气体的平均相对分子质量不随时间而变化
c.容器中气体的密度不随时间而变化
d.容器中气体的分子总数不随时间而变化
(3)在一个固定容积为5 L的密闭容器中充入0.20 mol SO2和0.10 mol O2,半分钟后达到平衡,测得容器中含SO3 0.18 mol,则v(O2)=__________mol·L-1·min-1;若继续通入0.20 mol SO2和0.10 mol O2,则平衡________________移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后,________mol<n(SO3)<________mol。
在化学反应中,能引发化学反应的分子间碰撞称之为有效碰撞,这些分子称为活化分子。使普通分子变成活化分子所需提供的最低能量叫活化能,其单位用kJ•mol-1表示。请认真观察下图,然后回答问题。
(1)图中反应是(填“吸热”或“放热”)反应,该反应(填“需要”或“不需要”)环境先提供能量,该反应的△H=(用含E1、E2的代数式表示)。
(2)对于同一反应,图中虚线(II)与实线(I)相比,活化能,因此反应速率,你认为最可能的原因是:。
(3)已知拆开1mol H-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为:____________________