X、Y、Z为常见的三种单质,Z是绿色植物光合作用的产物之一,A、B为常见化合物。它们在一定条件下可发生如图所示的反应(均是在非溶液中进行的反应):
(1)画出Z的原子结构示意图 ;
(2)当X为金属,Y为非金属时,A可能的电子式为 或 ;
(3)当X为非金属,Y为金属时,X可能的化学式为 或 ;
(4)当X与Y均为金属时,写出X与A反应的化学方程式 ;
(5)当X与Y均为非金属时,若X与Y同主族,写出X与A反应的化学方程式 ;若X与Y不在同一主族,写出X与A反应的化学方程式 。

(1)①用1.0 mol·L-1盐酸配制100 mL 0.10 mol·L-1盐酸,所需的玻璃仪器有量筒、
100 mL容量瓶、烧杯、、。
②用0.10 mol·L-1标准盐酸滴定未知浓度的烧碱溶液时,酸式滴定管初读教为0.10
mL,终读数如右图所示,则滴定所用盐酸体积为____。
(2)如右图所示,集气瓶内充满某混合气体,置于光亮处一段时间,
将滴管内的水挤入集气瓶,再打开止水夹,烧杯中的水会进入
集气瓶。该集气瓶中的气体可能是。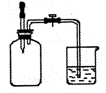
| A.CO、O2 |
| B.Cl2、CH4 |
| C.NO2、O2 |
| D.N2、H2 |
某研究性学习小组将下列装置如图连接,C、D、E、F、X、Y 都是惰性电极。向乙中滴入酚酞试液,将电源接通后,在F极附近显红色。试回答下列问题:
(1)电源A 极的名称是___________。
(2)甲装置中电解反应的 总化学方程式是
总化学方程式是
______________________________。
(3)如果收集乙装置中产生的气体,两种气体的体积比是_________ _。
_。
(4)欲用丙装置给铜镀银,G应该是______(填“铜”或“银”),电镀液是_______(填化
学式)溶液。
(5)装置丁中的现象是________________________________________。
(1)在粗制CuSO4·5H2O晶体中常含有杂质Fe2+。在提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+氧化为Fe3+,下列物质可采用的是________。
A. KMnO4 B. H2O2 C. Cl2水 D. HNO3
然后再加入适当物质调整至溶液pH=3.8,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+而不损
失CuSO4的目的,调整溶液pH可选用下列中的________。
A. NaOH B. NH3·H2O C. CuO D. Cu(OH)2
(2)甲同学怀疑调整至溶液pH=3.8是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可
以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp=8.0×10-38,
Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol·L-1
时就认为沉淀完全,设溶液中CuSO4的浓度为3.0 mol·L-1,则Cu(OH)2开始沉淀时溶液的
pH为________ ,Fe3+完全沉淀时溶液的pH为________,通过计算确定上述方案________(填
,Fe3+完全沉淀时溶液的pH为________,通过计算确定上述方案________(填
“可行”或“不可行”)。
用实验确定某酸HA是弱电解质。两同学的方案是:
甲:①称取一定量的HA配制0.1mol/L的溶液100mL;
②用pH试纸测出该溶液的pH值,即可证明HA是弱电解质。
乙:①用已知物 质的量浓度的HA溶液、盐酸,分别配制pH=1的两种酸溶液各100mL;
质的量浓度的HA溶液、盐酸,分别配制pH=1的两种酸溶液各100mL;
②分别取这两种溶液各10mL,加水稀释为100mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,
即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是__________。
(2) 甲方案中,说明HA是弱电解质的理由是测得溶液的pH____(选填<、>、=)1。
甲方案中,说明HA是弱电解质的理由是测得溶液的pH____(选填<、>、=)1。
乙方案中,说明HA是弱电解质的现象是_________。
a. 装盐酸溶液的试管放出H2的速率快。
b. 装HA溶液的试管放出H2的速率快。
c. 两个试管中产生H2的速率一样快。
(3)请你再提出一个合理而比较容易进行的方案(药品可任取),作简明扼要表述。
________________________________________________________________________。
已知一定温度和压强下,在容积为VL的密闭容器中充入1mol A和1mol B,保持恒温恒压下反应:A(g) + B(g)  C(g) △H<0。达到平衡时,C的体积分数为40%。试回答有关问题:
C(g) △H<0。达到平衡时,C的体积分数为40%。试回答有关问题:
(1)升温时,C的反应速率_______(填“加快”、“减慢”或“不变”)。
(2)若平衡时,保持容器容积不变,使容器内压强增大,则平衡__ _____。
_____。
| A.一定向正反应方向移动 | B.一定向逆反应方向移动 |
| C.一定不移动 | D.不一定移动 |
(3)若使温度、压强都保持和题干中的一样不变,在密闭容器中充入2mol A和2 mol B,则反应达到平衡时:A的转化率为_______(精确到0.01%),容器的容积为_______L。