下列说法不正确的是:
| A.煤、石油、天然气属于化石能源,太阳能、氢能、风能、地热能、海洋能属于新能源 |
| B.测试和调控溶液的pH对工农业生产、科学研究及日常生活和医疗保健都有重要意义。 |
| C.利用盐类的水解反应可以制备胶体、对饮用水进行净化,也可以获得纳米材料。 |
| D.化学电池必须回收处理,其主要目的就是回收碳棒再利用。 |
金属镁的制取主要有两种途径,大约60%的镁是从海水中提取的,其余来自于含镁丰富的矿石,比如菱镁矿(主要成分为MgCO3)。从不同途径获得镁的流程如下:
回答下列问题:
(1)试剂a的化学式是__________。
(2)加入试剂b发生反应的离子方程式是__________。
(3)操作A是蒸发浓缩、冷却结晶、__________。
(4)在电炉中参加反应的n(Cl2):n(焦炭)=1:1,则该反应的化学方程式是__________。
(5)上述制镁的流程中,为降低成本、减少污染可采取的措施是__________。(写出一种即可)
已知: C、
C、 分别按下式反应(燃烧):
分别按下式反应(燃烧):
① 放热
放热
② 放热
放热
③ 放热
放热
请回答:
(1)根据上述反应及数据,煤炭充分燃烧具有的优点是__________。
a. 放出热量多节约能源 b. 减少对环境的污染
(2)根据反应②,断开1 mol CO(g)与0.5 mol O2(g)中的化学键所吸收的能量,比形成1 mol CO2(g)中的化学键所放出的能量__________(填“多”或“少”)。
(3)在下图中画出反应③能量随反应过程的变化曲线。
(4)单质碳通过先与氧气反应生成CO(g),再与氧气反应生成CO2(g),所放出的热量之和与相同质量的碳与氧气完全反应生成CO2(g)所放出的热量的关系是__________(填“相等”或“不等”)。
乙烯是来自石油的重要有机化工原料,其产量通常用来衡量一个国家的石油化工发展水平。结合以下路线回答:
已知:
(1)上述过程中属于物理变化的是__________(填序号)。
①分馏②裂解
(2)A的官能团是__________。
(3)反应II的化学方程式是__________。
(4)D为高分子化合物,可以用来制造多种包装材料,其结构简式是__________。
(5)E是有香味的物质,在实验室可用下图装置制取。
①反应IV的化学方程式是__________。
②出于对安全的考虑,实验中应该采取的措施是__________。(写出一种即可)
(6)下列关于CH2=CH-COOH的说法正确的是__________。
①与CH3CH=CHCOOH互为同系物
②可以与NaHCO3溶液反应放出CO2气体
③在一定条件下可以发生取代、加成、氧化反应
①~⑧是元素周期表中的部分元素。
 族 族周期 |
IA |
0 |
||||||
| 1 |
① |
IIA |
IIIA |
IVA |
VA |
VIA |
VIIA |
|
| 2 |
② |
③ |
④ |
|||||
| 3 |
⑤ |
⑥ |
⑦ |
⑧ |
请回答:
(1)元素③④⑧的气态氢化物中最稳定的是__________(填化学式)。
(2)元素⑤和⑦的最高价氧化物对应水化物反应的离子方程式是__________。
(3)元素⑥和⑧形成的化合物的电子式是__________。
(4)某同学为了比较元素②和硅元素非金属性的相对强弱,用下图所示装置进行实验(夹持仪器已略去,气密性已检验)。请回答:
a. X是__________(填化学式),B装置的作用是__________。
b. 能说明元素②和硅元素非金属性强弱的实验现象是__________,相关的化学方程式是__________。同主族元素从上到下__________,得电子能力逐渐减弱,非金属性逐渐减弱。
(5)请设计实验比较元素⑥与⑦金属性的相对强弱__________。
为了研究外界条件对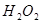 分解反应速率的影响,某同学在四支试管中分别加入
分解反应速率的影响,某同学在四支试管中分别加入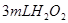 溶液,并测量收集
溶液,并测量收集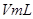 气体所需的时间,实验记录如下:
气体所需的时间,实验记录如下:
| 实验序号 |
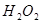 溶液浓度 溶液浓度 |
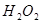 溶液温度 溶液温度 |
催化剂 |
所用时间 |
| ① |
5% |
20℃ |
2滴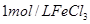 |
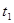 |
| ② |
5% |
40℃ |
2滴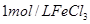 |
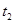 |
| ③ |
10% |
20℃ |
2滴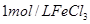 |
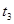 |
| ④ |
5% |
20℃ |
不使用 |
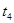 |
请回答:
(1)过氧化氢分解的化学方程式是__________。
(2)实验①②是研究__________对反应速率的影响。
(3)实验测得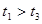 ,原因是__________。
,原因是__________。
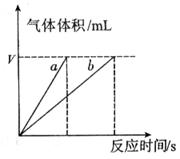
(4)实验①④的测定过程如下图,曲线a对应的实验序号是__________(填“①”或“④”)。