对于100mL 1mol/L盐酸与锌粒的反应,采取下列措施能使反应速率加快的是:①升高温度;②改用100mL 3mol/L盐酸;③改用300mL 1mol/L盐酸;④用等量锌粉代替锌粒;⑤滴入少量CuSO4溶液
| A.①③④⑤ | B.①②④⑤ | C.①②③④ | D.①②④ |
据央视报道,自2006年12月1日起在武汉九市进行车用乙醇汽油封闭推广行动。车用乙醇汽油是把变性燃料乙醇和汽油按一定比例混配形成的一种新型汽车燃料。经多项检测结果表明,它不影响汽车的行驶性能,还可以减少有害气体的排放量。在美国、巴西等国早已推广使用。下列有关乙醇汽油的说法正确的是( )
| A.乙醇汽油是一种纯净物 |
| B.乙醇汽油作燃料不会产生碳氧化物等有害气体,其优点是可以减少对环境的污染 |
| C.乙醇和汽油都可作溶剂,也可相互溶解 |
| D.乙醇和乙二醇互为同系物 |
甲烷是以碳原子为中心的正四面体结构,而不是正方形的平面结构,其理是
| A.甲烷中的四个键的键长、键角相等 | B.CH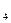 是分子晶体 是分子晶体 |
| C.二氯甲烷只有一种结构 | D.三氯甲烷只有一种结构 |
下列关于有机物的说法错误的是()
| A.CH4和Cl2在光照条件下反应的产物最多可能有四种 |
| B.CH3CH2OH是一种可再生的能源 |
| C.乙烯的结构简式为CH2=CH2 |
| D.从乙烯出发可经先加成后氧化制得乙醛 |
下列说法正确的是()
| A.苯与溴水混合振荡,水层颜色变浅,是由于苯与溴发生取代反应 |
| B.煤中含有苯和甲苯,可用先干馏后分馏的方法将它们分离出来 |
| C.蛋白质溶液中加入饱和(NH4)2SO4溶液后蛋白质会析出,再加水不溶解 |
| D.CH3COOH 和HCOOCH3是同分异构体 |
下列说法正确的是()
| A.“酒越陈越香”与酯化反应有关 |
| B.乙醇和油脂都能与氢氧化钠溶液反应 |
| C.淀粉、纤维素化学式均为(C6H10O5)n,互为同分异构体 |
| D.乙烯和苯均能与溴水发生加成反应 |