(1)在做淀粉水解实验过程中,若想证明淀粉已经水解,可以取水解液少许先中和后再加入 并加热至沸腾,现象为 ;若想证明淀粉只是部分水解,可以加入 ,现象为 。
(2)做银镜反应配制银氨溶液时,把 滴入到 只至 为止。
现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl-、SO42-、和NO3-的相互分离。相应的实验过程可用下图表示:
请回答下列问题:
⑴写出实验流程中下列物质的化学式
试剂X :沉淀A:沉淀B:
⑵上述实验流程中加入过量的Na2CO3的目的是。
⑶按此实验方案得到的溶液3中肯定含有(填化学式)杂质。
(Ⅰ)A、B、C三种无色可溶性盐分别是由Na+、Ag+ 、Ba2+、Cl—、NO3— 、CO32—中不同的阴、阳离子所组成。经实验A溶液、B溶液均可以与盐酸反应,其中A产生白色沉淀,B产生气泡。则A为、B为。将B和C的溶液混合反应的离子方程式为:。
(Ⅱ)有一包固体粉末,由CaCO3、Na2SO4、KNO3、BaCl2、CuSO4中的三种物质组成,取样品进行如下实验: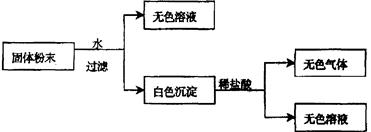
从实验可以判断,该固体粉末中一定不含有,它的组成可能是
或。
A、B、C、D、E 5瓶透明溶液,分别是HCl 、BaCl2、NaHSO4、Na2CO3、AgNO3溶液中的一种。
①A 与B反应有气体生成② B与C反应有沉淀生成③C与D反应有沉淀生成④D与E反应有沉淀生成⑤A与E反应有气体生成⑥在②和③的反应中生成的沉淀是同一种物质B是__________D是___________ (均填化学式)
下列物质:①铜丝②碳酸③氯化氢气体④稀硝酸⑤二氧化硫气体⑥氨水⑦蔗糖晶体⑧熔融氯化钠⑨氧化钠固体⑩硫酸铜晶体(用相应序号填空)
⑴上述物质可导电的是_________________⑵属于电解质的是__________________
(3)属于强电解质的是
(2分)已知Na与H2O发生反应:2Na +2H2O ="2NaOH" +H2↑,则4.6gNa溶于_______ g H2O中才能使溶液中Na+与H2O个数之比为1:10。