有A、B、C、D四种有机物,其组成均为含碳40%、氢6.67%、氧53.33%。A的蒸气对氢气的相对密度为15;B的相对分子质量为A的6倍;C、D的蒸气密度折算为标准状况下都是2.68g/L;A、B物质的水溶液都能发生银镜反应,其中B物质常用于制镜业;C物质的水溶液呈酸性,D物质呈中性。请按要求回答下列问题:
(1)写出A、B、C、D的结构简式和名称:
A___________________________________B____________________________________、
C____________________________________D________________________________
(2)写出D和新制氢氧化铜碱性悬浊反应的化学方程式: 。
短周期元素U、V、W、X、Y原子序数递增,V、W、X、Y四种元素依次相邻,可组成U2X、WU3、VU4型10电子化合物,也可组成U2Y、U2X2、W2U4、V2U6型18电子化合物。请据各情景回答问题。
⑴上述两种相对分子质量相等的18电子化合物在水溶液中相互反应,生成一种固体单质。写出有关化学方程式:。
⑵WU3在NaClO溶液中生成W2U4,写出有关离子方程式。
⑶U2X2和W2U4常温下均是无色液体,相互反应生成两种气体产物,均是大气成分。在pkPa、t℃时测得每生成36g U2X放出320kJ热量。写出有关热化学方程式:。
⑷W2U4—空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。电池放电时:负极的电极反应式是。
Ⅰ.中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、、。
Ⅱ.熔融盐燃料电池具有高的发电效率,因而受到重视。某燃料电池以熔融的K2CO3(其中不含O2-和HCO3-)为电解质,以丁烷为燃料,以空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极。该燃料电池负极电极反应式为:2C4H10+26CO32--52e- →34CO2+10H2O。试回答下列问题:
(1)正极电极反应式为。
(2)为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定。为此,必须在通入的空气中加入一种物质,加入的物质是,它来自。
(18分)我国第二代身份证采用的是具有绿色环保性能的PETG新材料,PETG新材料可以回收再利用,而且对周边环境不构成任何污染。这一材料是由江苏华信塑业发展有限公司最新研发成功的新材料,并成为公安部定点产地。PETG的结构简式为: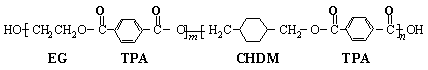
已知:
(1)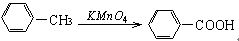
(2)RCOOR1 +R2OH RCOOR2 +R1OH (R、R1、R2表示烃基)
RCOOR2 +R1OH (R、R1、R2表示烃基)
这种材料可采用以下合成路线: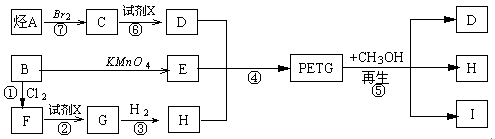
试回答下列问题:
(1)反应②⑥加入的试剂X是______________________
(2)⑤的反应类型是______________________
(3)写出结构简式:B:________H:__________I:____________
(4)合成时应控制的单体的物质的量
n(D)∶n(E)∶n(H)= _____∶______∶______(用m、n表示)
(5)写出化学方程式:
反应③:________________________________________________________
反应⑥:_______________________________________________________
现有A、B、C、D、E五种强电解质,它们在水中可电离产生下列离子(各种离子不重复)。
| 阳离子 |
H+、Na+、A13+、Ag+、Ba2+ |
| 阴离子 |
OH—、C1—、CO32—、NO3—、SO42- |
已知:①A、B两溶液呈碱性;C、D、E溶液呈酸性。②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有气体产生(沉淀包括微溶物,下同)。③D溶液与另外四种溶液反应都能产生沉淀;C只能与D反应产生沉淀。试回答下列问题:
(1)写出D为_________________
(2)将C溶液逐滴加入等体积、等物质量的浓度的A溶液中,反应后溶液中各种离子浓度由大到小的顺序为:_____________________。
(3)写出E溶液与过量的B溶液反应的离子方程式__________________________。
(4)已知:NaOH(aq)+HNO3(aq)=NaNO3(aq)+H2O(1);△H=-aKJ·mol-1。请写出B与C的稀溶液反应的热化学方程式______________________________
(5)在100 mL0.1 mol·L-1E溶液中,逐滴加入35 mL 2 mol·L-1NaOH溶液,最终得到沉淀物质的量为_____。
(12分)短周期的四种元素X、Y、Z、W,原子系数依次增大,Z原子最外层电子数是X、Y、W三种原子的最外层电子数之和,Z与X、Y、W三种元素形成原子个数之比为1:1的化合物分别是A.B.C,其中化合物C在空气中容易变质,请回答:
(1)写出Z的原子结构示意图______________________________。
(2)写出化合物YZ2电子式:______________空间构形为:_______________,
写出化合物C的电子式:_____________化学键类型有:_____________。
(3)写出化合物C在空气中变质的化学方程式:____________________