下列实验操作与预期实验目的或所得实验结论一致的是( )
| 选项 |
实验操作 |
实验目的或结论 |
| A |
将氯乙烷与氢氧化钠溶液共热一段时间,再向冷却后的混合液中滴加硝酸银溶液 |
检验水解产物中的氯离子 |
| B |
向丙醛溶液中加入新制的银氨溶液,用酒精灯直接加热 |
确定丙醛中是否含有醛基 |
| C |
向工业酒精中加入无水硫酸铜 |
确定工业酒精中是否含有水 |
| D |
电石与水反应,制得的气体直接通人酸性KMnO4溶液 |
检验制得的气体是否为乙炔 |
下列有关计算的分析正确的是
| A.某溶液100mL,其中含硫酸0.03mol,硝酸0.04mol,若在该溶液中投入1.92 g铜粉微热,反应后放出一氧化氮气体约为0.015mol |
| B.室温时,在容积为a mL的试管中充满NO2气体,然后倒置在水中到管内水面不再上升时为止;再通入b mL O2,则管内液面又继续上升,测得试管内最后剩余气体为c mL,且该气体不能支持燃烧.则a、b的关系是a=4b+c |
C.已知某温度Ksp(Ag2S)=6×10-50,Ksp(AgCl)=2×10-6,则2AgCl(s)+S2-(aq) Ag2S(s)+2Cl-(aq)的平衡常数约为6.7×10-37 Ag2S(s)+2Cl-(aq)的平衡常数约为6.7×10-37 |
D.在25 ℃下,将2a mol·L-1的氨水与0.02 mol·L-1的盐酸等体积混合,反应完全时溶液中c(NH4+)=c(Cl-),则用含a的代数式表示NH3·H2O的电离常数  |
类推的思维方法在化学学习与研究中经常用到,但有时会产生错误的结论。因此,推出的结论最终要经过实践的检验才能决定其是否正确。以下几种类推结论中,正确的是
| A.IVA族元素氢化物沸点顺序是:GeH4>SiH4>CH4;则VA族元素氢化物沸点顺序也是:AsH3>PH3>NH3 |
| B.第二周期元素氢化物的稳定性顺序是:HF>H2O>NH3;则第三周期元素氢化物的稳定性顺序也是:HCl>H2S>PH3 |
| C.Fe3O4可以写成FeO·Fe2O3;Pb3O4也可以写成PbO·Pb2O3 |
| D.NaHSO4与NaHSO3溶于水显酸性,则所有酸式盐溶于水显酸性 |
A+、B+、C-、D-四种离子两两组成四种可溶性盐,其中AC和BD的盐溶液的pH=7,BC盐溶液pH>7,则下列说法正确的是:
A、AD盐溶液pH>7
B、酸的电离程度一定是HD<HC
C、碱的电离程度一定是AOH>BOH
D、在AC盐溶液中c(A+)+ c(AOH)= c(C-)+ c(HC)
由一种阳离子和两种酸根离子组成的盐称混盐。下列关于混盐Na4S2O3的有关判断,不正确的是
| A.该混盐水溶液呈碱性 |
| B.该混盐与H2SO4反应有气体生成 |
| C.该混盐溶液加入BaCl2可以生成白色沉淀 |
| D.该混盐在酸性条件下可生成S,每产生32g S转移2NA个电子 |
已知某有机物X的结构简式如图所示,下列有关叙述不正确的是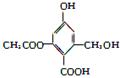
| A.X的化学式为C10H10O6 |
| B.X在一定条件下能与FeCl3溶液发生显色反应 |
| C.1 mol X分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别为3 mol、4 mol、1 mol |
| D.X在一定条件下能发生消去反应和酯化反应 |