短周期元素A、B、C、D、E、F六种元素,它们的原子序数由A到F依次增大。在周期表中,A的原子半径最小。B元素的原子最外层电子数是内层电子数的两倍,C为地壳中含量最多的元 素,D是原子半径最大的短周期主族元素, D单质燃烧时呈现黄色火焰, D的单质在高温下与C的单质充分反应, 可以得到与E单质颜色相同的淡黄色固态化合物。D与F形成的离子化合物DF是常用的调味品。试根据以上叙述回答:
素,D是原子半径最大的短周期主族元素, D单质燃烧时呈现黄色火焰, D的单质在高温下与C的单质充分反应, 可以得到与E单质颜色相同的淡黄色固态化合物。D与F形成的离子化合物DF是常用的调味品。试根据以上叙述回答:
(1)元素名称: A B D
(2)E在周期表中的位置: ____________________
(3)F离子结构示意图: __________________
(4)A、B组成的最简单化合物的名称是___________
(5)用电子式表示BC2的形成过程:
(6)C单质与D单质在常温下反应的产物的电子式_______________________
(7)C单质与D单质在点燃条件下反应的产物W中所含化学键类型为__________ ____,将W溶于水的化学方程式______________________ ____________,W的用途有______________ (填一种)
(8)能说明E的非金属性比F的非金属性____(填“强”或“弱”)的事实是: ______________________ (举一例)。
 化合物
是一种香料,存在于金橘中,可用如下路线合成:
化合物
是一种香料,存在于金橘中,可用如下路线合成:


已知:
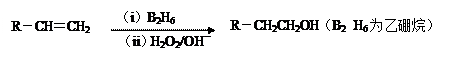

 回答下列问题:
回答下列问题: (1)11.2
(标准状况)的烃
在氧气中充分燃烧可以产生88
和45
。
(1)11.2
(标准状况)的烃
在氧气中充分燃烧可以产生88
和45
。 的分子式是
的分子式是
 (2)
和
均为一氯代烃,它们的名称(系统命名)分别为;
(2)
和
均为一氯代烃,它们的名称(系统命名)分别为; (3)在催化剂存在下1
与2
反应,生成3-苯基-1-丙醇。F的结构简式是
(3)在催化剂存在下1
与2
反应,生成3-苯基-1-丙醇。F的结构简式是
 (4)反应①的反应类型是;
(4)反应①的反应类型是; (5)反应②的化学方程式为
(5)反应②的化学方程式为
 (6)写出所有与
具有相同官能团的
的芳香类同分异构体的结构简式:
(6)写出所有与
具有相同官能团的
的芳香类同分异构体的结构简式:

 浓
和木炭在加热时发生反应的化学方程式是
浓
和木炭在加热时发生反应的化学方程式是
 ↑
↑
↑
↑ 请从下图中选用所需的仪器(可重复选用)组成一套进行该反应并要检出反应产物的装置。现提供浓
、木炭和酸性
溶液,其他固、液试剂自选。(连接和固定仪器所用的玻璃管、胶管、铁夹、铁架台及加热装置等均略去)
请从下图中选用所需的仪器(可重复选用)组成一套进行该反应并要检出反应产物的装置。现提供浓
、木炭和酸性
溶液,其他固、液试剂自选。(连接和固定仪器所用的玻璃管、胶管、铁夹、铁架台及加热装置等均略去)
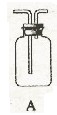


 将所选的仪器连接顺序由上至下依次填入下表,并写出该仪器中应加试剂的名称及其作用。
将所选的仪器连接顺序由上至下依次填入下表,并写出该仪器中应加试剂的名称及其作用。
选用的仪器 (填字母) (填字母) |
加入的试剂 |
作用 |
     |
   |
   |

化合物
相对分子质量为86,碳的质量分数为55.8%,氢为7.0%,其余为氧。
的相关反应如下图所示:

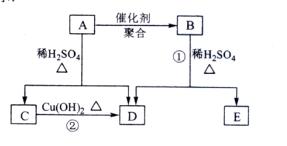

 已知
(烯醇)不稳定,很快转化为
。
已知
(烯醇)不稳定,很快转化为
。
 根据以上信息回答下列问题:
根据以上信息回答下列问题:
 (1)
的分子式为;
(1)
的分子式为;
 (2) 反应②的化学方程式是;
(2) 反应②的化学方程式是;
 (3)
的结构简式是;
(3)
的结构简式是;
 (4) 反应①的化学方程式是;
(4) 反应①的化学方程式是;
 (5)
有多种同分异构体,写出四个同时满足(i)能发生水解反应(ii)能使溴的四氯化碳溶液褪色两个条件的同分异构体的结构简式:;
(5)
有多种同分异构体,写出四个同时满足(i)能发生水解反应(ii)能使溴的四氯化碳溶液褪色两个条件的同分异构体的结构简式:;
 (6)
的另一种同分异构体,其分子中所有碳原子在一条直线上,它的结构简式为。
(6)
的另一种同分异构体,其分子中所有碳原子在一条直线上,它的结构简式为。

 现有
、
、
、
、
、
六种化合物,已知它们的阳离子有
,
现有
、
、
、
、
、
六种化合物,已知它们的阳离子有
, 阴离子有
,现将它们分别配成
的溶液,进行如下实验:
阴离子有
,现将它们分别配成
的溶液,进行如下实验:
①
 测得溶液
、
、
呈碱性,且碱性为
;
测得溶液
、
、
呈碱性,且碱性为
;
②
 向B溶液中滴加稀氨水,先出现沉淀,继续滴加氨水,沉淀消失;
向B溶液中滴加稀氨水,先出现沉淀,继续滴加氨水,沉淀消失;
③
 向D溶液中滴加
溶液,无明显现象;
向D溶液中滴加
溶液,无明显现象;
④
 向F溶液中滴加氨水,生成白色絮状沉淀,沉淀迅速变成灰绿色,最后变成红褐色。
向F溶液中滴加氨水,生成白色絮状沉淀,沉淀迅速变成灰绿色,最后变成红褐色。
 根据上述实验现象,回答下列问题:
根据上述实验现象,回答下列问题:
(1)
 实验②中反应的化学方程式是
实验②中反应的化学方程式是
 ;
;
 (2)
溶液是,判断依据是
(2)
溶液是,判断依据是

 (3)写出下列四种化合物的化学式:
、
、
(3)写出下列四种化合物的化学式:
、
、
、
.

 某温度时,在2L密闭容器中气态物质
和
反应生成气态物质
,它们的物质的量随时间的变化如表所示。
某温度时,在2L密闭容器中气态物质
和
反应生成气态物质
,它们的物质的量随时间的变化如表所示。
 (1)根据左表中数据,在右图中画出
、
、
的物质的量(
)随时间(
)变化的曲线:
(1)根据左表中数据,在右图中画出
、
、
的物质的量(
)随时间(
)变化的曲线:
| t/min |
X/mol |
Y/mol |
Z/mol |
| 0 |
1.00 |
1.00 |
0.00 |
| 1 |
0.90 |
0.80 |
0.20 |
| 3 |
0.75 |
0.50 |
0.50 |
| 5 |
0.65 |
0.30 |
0.70 |
| 9 |
0.55 |
0.10 |
0.90 |
| 10 |
0.55 |
0.10 |
0.90 |
| 14 |
0.55 |
0.10 |
0.90 |


 (2) 体系中发生反应的化学方程式是;
(2) 体系中发生反应的化学方程式是;
 (3) 列式计算该反应在0-3min时间内产物
的平均反应速率:;
(3) 列式计算该反应在0-3min时间内产物
的平均反应速率:;
 (4) 该反应达到平衡时反应物
的转化率
等于;
(4) 该反应达到平衡时反应物
的转化率
等于;
 (5) 如果该反应是放热反应。改变实验条件(温度、压强、催化剂)得到Z随时间变化的曲线①、②、③(如右图所示)则曲线①、②、③所对应的实验条件改变分别是:
(5) 如果该反应是放热反应。改变实验条件(温度、压强、催化剂)得到Z随时间变化的曲线①、②、③(如右图所示)则曲线①、②、③所对应的实验条件改变分别是:
 ①②③
①②③



