电解法制碱的主要原料是饱和食盐水,由于粗盐水中含有泥沙、Ca2+、Mg2+、Fe3+、SO等杂质,不符合电解要求,因此必须经过精制.某同学设计了一种制备 精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
步骤1:取一定量的粗盐,置于烧杯中,加入足量的水,配成粗盐水;
步骤2:向粗盐水中加入除杂试剂,然后进行过滤,滤去不溶物,再向滤液中加入盐酸
调节盐水的pH;
步骤3:将得到的溶液蒸发浓缩、冷却、结晶、过滤、烘干即得精盐;
请回答以下问题:
(1)上述实验中的过滤操作需要烧杯、____________、____________等玻璃仪器.
(2)步骤2中常用Na2CO3、NaOH、BaCl2作为除杂试剂,则加入除杂试剂的顺序为:
________________.
(3)步骤2中,判断加入BaCl2已过量的方法是:_______________________________
_______________________.
(4)步骤2中,若先用盐酸调节pH再过滤,将会对实验结果产生影响,其原因是
________________________________________________________________________. (5)为检验精盐纯度,需配制150 mL 0.2 mol/L NaCl(精盐)溶液,右图是该
(5)为检验精盐纯度,需配制150 mL 0.2 mol/L NaCl(精盐)溶液,右图是该
同学转移溶液的示意图,图中的两处错误是:
________________________________________________
________________________________________________.
若在定容时仰视,则所配溶液的浓度_____________________________________
0.2 mol/L(填“大于”或“小于”);若定容不慎超过刻度线,应采用的处理方法是: ________________________________________________________________________.
某活动小组设计了以下实验,其实验目的是观察两份完全相同的铁粉与铝粉的混合物分别与足量盐酸和NaOH溶液反应的删程;测定部分数据对混合物的成分进行定量分析。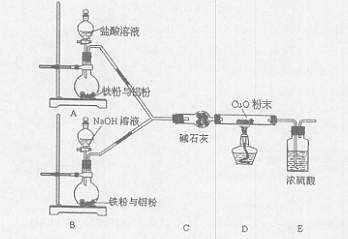
请回答:
(1)碱石灰的作用是。
(2)下列操作进行的顺序由先到后的是(填序号)。
①同时打开A、B中分液漏斗的活塞,分别加人足量试剂
②检查装置的气密性③点燃酒精灯
④装入药品⑤熄灭酒精灯
⑥同时关闭A、B中分液漏斗的活塞
(3)写出B装置中发生反应的离子方程式:。
(4)写出装置A、B中实验现象的不同点。
(5)该装置不够完善,还需增加的装置为。
(6)已知反应前金属混合物的质量,发生反应后测定混合物成分的最简单方法是。
(7)若混合金属中铁与铝的质量比为28:27,则充分反应后,A和B两烧瓶中转移电子总数之比为。
已知非金 属单质硫(S)是淡黄色固体粉末,难溶于水。为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:
属单质硫(S)是淡黄色固体粉末,难溶于水。为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题: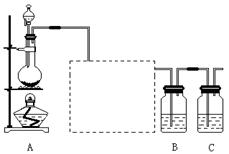
(1)装置A的分液漏斗中盛装的试剂是,烧瓶中加入的试剂是。
(2)虚线框内的实验装置图,所加试剂为,说明装置的作用。
(3 )装置B中盛放的试剂是(选填下列所给试剂的代码),实验现象为,
)装置B中盛放的试剂是(选填下列所给试剂的代码),实验现象为,
化学反应方程式是,
该反应属于四种基本反应类型中的反应。
A.Na2S溶液 B.Na2SO3溶液 C.Na2SO4溶液
(4)从原子结构的角 度简要分析氯元素的非金属性比硫元素的非金属性强的原因。
度简要分析氯元素的非金属性比硫元素的非金属性强的原因。
(5)还有哪些事实能够说明氯元素的非金属性比硫元素的非金属性强(试举一例)。
(6)装置C中盛放烧碱溶液,目的是吸收反应后剩余的气体,防止污染空气。在该反应中,Cl元素的化合价既有升高又有降低,即在反应中Cl元素的原子既能获得电子也能失去电子,能否说氯元素既具有金属性又具有非金属性?简述你的理由。
。
(12分)下图是一个制取氯气并以氯气为原料进行某些反应的装置。(夹持和加热装置省略)。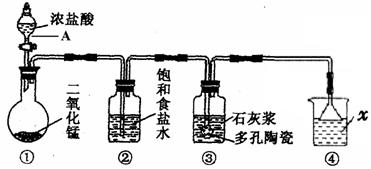
(1)写出图中仪器A的名称:。
(2)装置中x试剂为;装置中饱和食盐水的作用是。
(3)装置③中发生反应的化学方程式为。
(4)若将生成的C12通入淀粉碘化钾无色溶液中,可观察到溶液变成色,反应的离子方程式为。
某学习小组利用铁与稀硫酸的反应,进行“探究影响化学反应速率因素”的实验。结果如下表:
| 实验 序号 |
铁的质量/g |
铁的 形态 |
V(H2SO4) /mL |
c(H2SO4) /mol·L-1 |
反应前溶液 的温度/℃ |
金属完全消 失的时间/s |
| 1 |
0.10 |
片状 |
50 |
0.8 |
20 |
200 |
| 2 |
0.10 |
粉状 |
50 |
0.8 |
20 |
25 |
| 3 |
0.10 |
片状 |
50 |
1.0 |
20 |
125 |
| 4 |
0.10 |
片状 |
50 |
1.0 |
35 |
50 |
请分析上表信息,回答下列问题。
(1)实验1、2 表明 对反应速率有影响,其规律是 。
(2)仅表明反应物浓度对反应速率产生影响的实验有 (填实验序号)。
(3)该探究实验中,影响反应速率的因素还有 ,体现该影响因素的实验有 (填实验序号)。
(4)进行实验3时,若将稀硫酸改为50 mL 2.0 mol·L-1 盐酸(其他条件不变),发现:放出气泡的速率,盐酸明显比硫酸快。你认为可能的原因是。
(忽略温度对反应速率的影响)
某学生进行蔗糖水解的实验,并检验水解产物中是否含有葡萄糖。它的操作如 下:①取少量蔗糖加适量水配成溶液
下:①取少量蔗糖加适量水配成溶液
②在蔗糖溶液中加入3~5滴稀H2SO4
③将混合液煮沸几分钟,冷却
④在冷却后的溶液中加入银氨溶液,水浴加热,其实验结果没有银镜产生。其原因是__________。
| A.蔗糖尚未水解 | B.加热时间不够 |
| C.煮沸后的溶解中没有加碱中和其酸性 | D.蔗糖水解的产物中没有葡萄糖 |
上述实验的正确操作是.