有一种白色粉末由等质量的两种物质混合而成,分别取适量该白色粉末置于三支试管中进行实验。
(1)逐滴加入6mol·L-1盐酸,同时不断振荡试管,有气泡产生,反应结束后得到无色透明溶液
(2)加热试管中的白色粉末,试管口有水滴凝结
(3)逐滴加入6mol·L-1硫酸,同时不断振荡试管,有气泡产生,反应结束后试管口还有白色难溶物
下列混合物中符合以上实验现象的是 ( )
| A.NaHCO3、AgNO3 |
| B.BaCl2、MgCO3 |
| C.NH4HCO3、MgCl2 |
| D.CaCl2·6H2O、Na2CO3 |
不属于“雾霾”等灾害性天气治理的措施是
| A.外出时使用PM2.5口罩,减少有害物质的吸入 |
| B.改燃煤为燃气,可减少废气中SO2等有害物质的量 |
| C.利用太阳能、潮汐能、风力发电,以获取清洁能源 |
| D.使用“乙醇汽油”,减少汽车尾气中有害气体的排放 |
0.02 mol FeS2与一定浓度的硝酸完全反应,Fe元素和S元素全部转化为 和
和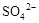 ,同
,同
时产生氮的氧化物(NO、NO2、N2O4)混合气体共0.25 mol,该混合气体的平均相对分子质量可能是
| A.30 | B.46 | C.50 | D.66 |
常温下,向20.00mL 0.1000 mol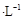 (NH4)2 SO4溶液中逐滴加入0.2000 mol
(NH4)2 SO4溶液中逐滴加入0.2000 mol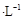 NaOH时,溶液的pH与所加NaOH溶液体积的关系如下图所示(不考虑挥发)。
NaOH时,溶液的pH与所加NaOH溶液体积的关系如下图所示(不考虑挥发)。
下列说法正确的是
| A.点a所示溶液中:c(NH4+)>c(SO42-)>c(H+)>c(OH-) |
| B.点b所示溶液中:c(NH4+)=c(Na+)>c(H+)=c(OH-) |
| C.点c所示溶液中:c(SO42)+ c(H+)= c(NH3·H2O )+ c(OH-) |
| D.点d所示溶液中:c(SO42)>c(NH3·H2O )>c(OH-)>c(NH4+) |
下列除杂分离方法正确的是
| 选项 |
物质 |
杂质 |
所用试剂 |
分离方法 |
| A. |
KCl |
CaCl2 |
Na2CO3溶液、盐酸 |
过滤 |
| B. |
CH3CH2OH |
CH3COOH |
CaO |
蒸馏 |
| C. |
NaCl |
NH4Cl |
NaOH |
蒸干 |
| D. |
N2 |
O2 |
铜网 |
加热 |
下列实验过程中产生的现象与所给图形相符合的是( )
| A.往乙酸中通入氨气 |
B.往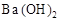 溶液中滴加硫酸 溶液中滴加硫酸 |
| C.往氢硫酸溶液中通入氯气 |
| D.往NaOH溶液中通入过量CO2 |