为了证明在实验室制备Cl2的过程中会有水蒸气和HCl挥发出来,甲同学设计了如下图所示的实验装置,按要求回答问题。
(1)请根据甲同学的意图,连接相应的装置,接口的顺序:b接______,_______接______,______接a。
(2)U形管中所盛试剂的化学式为_________________。
(3)装置③中CCl4的作用是________________。
(4)乙同学认为甲同学实验有缺陷,不能证明最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在某两个装置之间再加装置⑤。你认为装置⑤应加在_______之间(填装置序号)。瓶中可以放入______________________________________________________。
(5)丙同学看到甲同学设计的装置后提出无需多加装置,只需将原来烧杯中AgNO3溶液换成其它溶液。你认为可将溶液换成_____________,如果观察到_____________________的现象,则证明制Cl2时有HCl挥发出来。
(16分) 某研究性小组借助A-D的仪器装置(可以重复使用)完成有关实验
某研究性小组借助A-D的仪器装置(可以重复使用)完成有关实验

 【实验一】收集NO气体。
【实验一】收集NO气体。 (1)用装置A收集NO气体,正确的操作是(填序号)。
(1)用装置A收集NO气体,正确的操作是(填序号)。 a.从①口进气,用排水法集气 b.从①口进气,用排气法集气
a.从①口进气,用排水法集气 b.从①口进气,用排气法集气 c.从②口进气,用排水法集气 d..从②口进气,用排气法集气
c.从②口进气,用排水法集气 d..从②口进气,用排气法集气 【实验二】净化用浓盐酸与KMnO4反应得到的Cl2。
【实验二】净化用浓盐酸与KMnO4反应得到的Cl2。
(2)请参照装置A,画出净化Cl2装置图,标明所盛的药品,标注气体的流动方向。
【实验三】为了探究镀锌薄铁板上的锌的质量分数w(Zn)和镀层厚度,查询得知锌易溶于强碱:Zn+2NaOH=Na2ZnO2+H2↑ 据此,截取面积为S的双面镀锌薄铁板试样,剪碎、称得质量为m1 g。用NaOH溶液作试剂,拟出下列实验方案并进行相关实验。 方案甲:通过测量试样与碱溶液反应生成的氢气体积来实现探究目标。
方案甲:通过测量试样与碱溶液反应生成的氢气体积来实现探究目标。
(3) 选用和(填仪器标号)两个装置进行实验。
选用和(填仪器标号)两个装置进行实验。
(4) 测得充分反应后生成氢气的体积为VL(标准状况),w(Zn)=。
测得充分反应后生成氢气的体积为VL(标准状况),w(Zn)=。
(5) 计算镀层厚度,还需要检索的一个物理量是。
计算镀层厚度,还需要检索的一个物理量是。
(6) 若装置B中的恒压分液漏斗改为普通分液漏斗,测量结果将(填“偏大”、“偏小”或“无影响”)。
若装置B中的恒压分液漏斗改为普通分液漏斗,测量结果将(填“偏大”、“偏小”或“无影响”)。 方案乙:通过称量试样与碱反应前后的质量实现探究目标。选用仪器C做实验,试样经充分反应,滤出不溶物、洗涤、烘干,称得其质量为m2g
方案乙:通过称量试样与碱反应前后的质量实现探究目标。选用仪器C做实验,试样经充分反应,滤出不溶物、洗涤、烘干,称得其质量为m2g ;
;
(7)w(Zn)=。
(12分)某同学准备用CuSO4·5H2O配制480 mL 1 mol/L的溶液。
⑴该同学选用的容量瓶容积的规格是mL;
⑵玻璃棒在该实验中有重 要的用途,分别是和;
要的用途,分别是和;
⑶配制好的溶液呈 色。该同学还想通过实验分别证实溶质中含有Cu2+、SO42-,请你帮他想想办法,选择适当的试剂(写化学式),并写出其相应的离子方程式。
色。该同学还想通过实验分别证实溶质中含有Cu2+、SO42-,请你帮他想想办法,选择适当的试剂(写化学式),并写出其相应的离子方程式。
| 溶质 |
加入试剂 |
离子方程式 |
| Cu2+ |
||
| SO42- |
⑷物质的量浓度误差分析:(填偏高、偏低、无影响)
①若容量瓶洗净后未干燥,残留少量水,则所配制的溶 液浓度将
液浓度将 ;
;
②定容时,若眼睛俯视,则所配制的溶液浓度将。
在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应。应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”。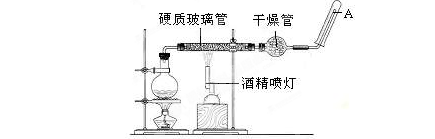
请回答该实验中的问题。
(1)写出该反应的反应方程式:;并指明该氧化还原反应的还原剂是,氧化剂是,假设有1mol氧化剂参加反应,转移的电子数的物质的量为。
(2)圆底烧瓶中盛装的水,该装置受热后的主要作用是;烧瓶底部放置了几片碎瓷片,碎瓷片的作用是。
(3)酒精灯和酒精喷灯点燃的顺序是,为什么?。
(4)干燥管中盛装是的物质是,作用是 。
。
(5)某次实验后,取硬质玻璃管中的固体物质少量,溶于足量稀盐酸,再滴加KSCN溶液。溶液颜色无明显变化,试解释原因。
影响化学反应速率的因素很多,某课外兴趣小组用实验的方法通过图1所示装置研究反应速率的有关问题。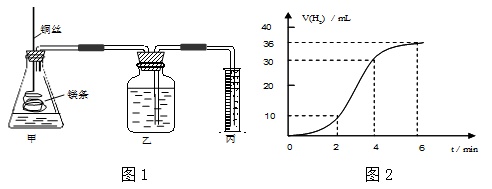
(1)取一段镁条,用砂纸擦去表面的氧化膜,使镁条浸入锥形瓶内足量的稀盐酸中。足量镁条与一定量盐酸反应生成H2的量与反应时间的关系曲线如图2所示。
①请根据实验中现象并结合图2中数据回答0到6分钟内哪一段速率最快。
A: 0—2 分钟 B: 2—4 分钟 C: 4—6分钟
②并请简述速率出现这种情况的其原因:
(2)某同学发现,纯度、质量、表面积都相同的两铝片与H+浓度相同的盐酸和硫酸在同温同压下反应时产生氢气的速率差别很大,铝和盐酸反应速率更快。他决定对其原因进行探究。填写下列空白:
①该同学认为:由于预先控制了反应的其他条件,那么,两次实验时反应的速率不一样的原因,只有以下五种可能:
原因Ⅰ:Cl-对反应具有促进作用,而SO2- 4对反应没有影响;
原因Ⅱ:Cl-对反应没有影响,而SO2- 4对反应具有阻碍作用;
原因Ⅲ:____________________________________________________;
原因Ⅳ:Cl-、SO2- 4均对反应具有促进作用,但Cl-影响更大;
原因Ⅴ:_______________________________________。
②该同学设计并进行了两组实验,即得出了正确结论。他取了两片等质量、外形和组成相同、表面经过砂纸充分打磨的铝片,分别放入到盛有同体积、c(H+)相同的稀硫酸和盐酸的试管(两试管的规格相同)中:
a.在盛有硫酸的试管中加入少量NaCl或KCl固体,观察反应速率是否变化;
b.在盛有盐酸的试管中加入少量Na2SO4或K2SO4固体,观察反应速率是否变化。
若观察到实验a中________________________,实验b中________________________,则说明原因Ⅰ是正确的。依次类推。该同学通过分析实验现象,得出了结论:Cl-对反应具有加速作用。
( 16分)某兴趣小组拟利用如下图装置探究验证干燥的Cl2和潮湿的C l2有无漂白性。
l2有无漂白性。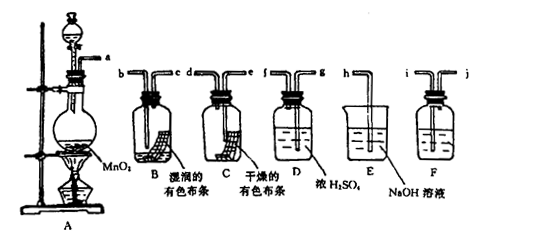
回答下列问题:
(1)A装置中的主要玻璃仪器有:导管、酒精灯、圆底烧瓶、。
A装置中发生反应的化学方程式是。
F装置中的试剂应为,作用为。
(2)按气体从左向右流向将各装置依次连接起来(填接口标号): a接,
接,接,接,接 。
。
(3)通入Cl2后,从集气瓶A、B中 红色布条的现象可得出的结论是
红色布条的现象可得出的结论是
;其中发生的反应的化学方程式为。
(4)为了确证是HClO使湿润的红色布条褪色,你认为还应增加的实验是
。
(5)烧杯E中发生反应的化学方程式为。
(6)为保证实验安全,当氯气以每分钟1.12L(标准状况)的流速匀速通入时,若实验需耗时4分钟,小烧杯中盛4 mol·L-1的NaOH溶液的体积至少应为mL。