1962年,英国青年化学家巴特莱特将PtF6和Xe 按等物质的量之比在室温下混合后首次制得含有化学键的稀有气体化合物六氟合铂酸氙: Xe + PtF6 → XePtF6有关此反应的下列叙述中,正确的是
| A.Xe是氧化剂 | B.PtF6是氧化剂 |
| C.PtF6既是氧化剂,又是还原剂 | D.该反应是非氧化还原反应 |
天然碱的组成可以用aNa2CO3·bNaHCO3·cH2O(a、b、c为整数)表示。通过以下实验测定某天然碱的化学式,将质量为12.45 g的某天然碱溶于水,逐滴滴加某浓度的稀盐酸,产生气体的体积与加入盐酸的体积(标准状况)的关系如下表所示:
| 盐酸体积(mL) |
20 |
40 |
60 |
80 |
| 产生气体体积(mL) |
0 |
560 |
1680 |
2520 |
下列说法错误的是
A.加入盐酸体积小于20 mL时,体系发生的离子反应为: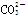 +H+===
+H+===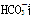
B.加入盐酸体积为50 mL时,产生气体(标准状况)的体积为1120mL
C.本实验使用盐酸的浓度为2.5 mol·L-1
D.该天然碱的化学式为Na2CO3·2NaHCO3·2H2O
室温下,在0.2 mol·L-1 Al2(SO4)3,溶液中,逐滴加入1.0 mol·L-1 NaOH溶液,实验测得溶液pH随NaOH溶液体积变化曲线如图,下列有关说法正确的是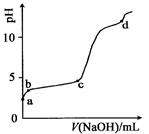
A.a点时,溶液呈酸性的原因是Al3+水解,离子方程式为:Al3++3OH- Al(OH)3 Al(OH)3 |
| B.a~b段,溶液pH增大,Al3+浓度不变 |
| C.b~c段,加入的OH-主要用于生成Al(OH)3沉淀 |
| D.d点时,Al(OH)3沉淀开始溶解 |
利用下图所示实验装置测定气体摩尔体积,所用药品为1g锌粒和10 mL 0.5 mol·L-1硫酸溶液,相关叙述正确的是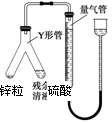
| A.实验时,将硫酸溶液倾斜倒入锌粒中 |
| B.实验时,量气管压入漏斗的水过多而溢出,不影响实验 |
| C.实验时,待体系温度降低到0℃时方可进行读数 |
| D.实验时,用CCl4代替水,测得氢气的体积更准确 |
下列有关实验原理或实验操作正确的是
某同学探究氨和铵盐的性质,相关实验操作及现象描述正确的是
| A.加热NH4Cl晶体制备氨气 |
| B.将蘸有浓氨水和浓硝酸的玻璃棒靠近,观察到白烟 |
| C.将氨水缓慢滴入AlCl3溶液中,研究Al(OH)3的两性 |
| D.室温下测定等浓度氨水和NaOH溶液的pH,比较N和Na的金属性强弱 |