二氧化碳又名碳酸气,具有较高的民用和工业价值,在多种领域有着广泛的应用。目前,二氧化碳在棚菜气肥、蔬菜(肉类)保鲜、生产可降解塑料等领域也展现良好的发展前景。二氧化碳是一种无色无味的气体,无毒、不导电并且没有可燃性。但是金属镁在点燃的条件下可以在二氧化碳气体中燃烧。其中还原产物是碳。
Ⅰ.①氧化产物是
②请写出化学反应方程式,并用双线桥法表示该反应的电子转移总 数
数
Ⅱ.CO2气体与碱溶液反应时,用量不同其生成的产物不同。
取两份等物质的量浓度等体积的Ca(OH)2的溶液,一份通入过量CO2,生成沉淀的物质的量(n)和通入CO2体积(V)的关系如图所示
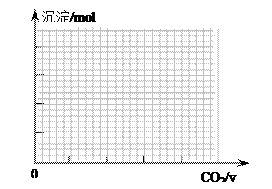
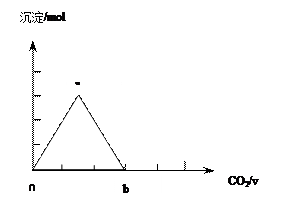
写出沉淀变化由a到b的离子方程式:
Ⅲ.另一份先加入少量的KOH固体溶解,再将过量CO2通入KOH和Ca(OH)2的混合溶液中,请绘图表示出生成沉淀的物质的量(n)和通入CO2体积(V)的关系;
 并写出与上图中不同曲线处对应的离子反应方程式 ;
并写出与上图中不同曲线处对应的离子反应方程式 ;
。
A为单质,B、C、D、E为与A含有相同元素的化合物,它们之间有如下转化关系: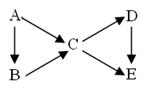
(1)若上图中B、C均为氧化物、D、E均为盐,则A可能是__________。
①Na②N2 ③C④S
(2)若五种物质的焰色反应均为黄色,其中C、D、E的水溶液
均显碱性,且等浓度时碱性C>D>E,B可做生氧剂, 则B中含有的化学键类型为__________________;
则B中含有的化学键类型为__________________;
A转化成C的离子方程式为: ________________________________,
D转化成E的离子方程式为____________________ ___________________。
___________________。
(3)若常温下B、C、D均为气体,且B气体能使湿润的红色石蕊试纸变蓝
①在工业上生产B气体时为了加快反应速率应选择的条件是______________,其中能提高反应物的转化率的条件是___________。
②C、D是汽车尾气中的有害成分,用NaOH溶液吸收可消除污染,反应的化学方程式为__________________________________。
铁与HNO3 作用时,还原产物除与HNO3浓度有关外,还与温度有关。已知铁与冷的稀HNO3反应时,主要还原产物为NO气体;与热的稀HN03反应时,主要还原产物为N2O气体;当HNO3更稀时,其重要还原产物是NH4+。现有铁与稀 HNO3的作用,请分析下图,回答有关问题。
作用时,还原产物除与HNO3浓度有关外,还与温度有关。已知铁与冷的稀HNO3反应时,主要还原产物为NO气体;与热的稀HN03反应时,主要还原产物为N2O气体;当HNO3更稀时,其重要还原产物是NH4+。现有铁与稀 HNO3的作用,请分析下图,回答有关问题。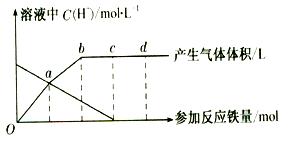
假设曲线的各段内只有一种还原产物,。
(1)0点到a点的还原产物是。
(2)a点到b点的还原产物是____,其原因是。
(3)试完成b点到c点的反应方程式:
口Fe+口HNO3——口Fe( NO3)3+口[ ]+口H20。
(4)反应过程中,到达点时,HN03已完全反应。
(5)已知达到d点时反应结束,此时溶液中的主要阳离子是。
( 6)c点和d点参加反应的铁的物质的量之比是。
6)c点和d点参加反应的铁的物质的量之比是。
某溶液仅含下表离子中的5种(不考虑水的电离及离子的水解)且各种离子物质的量均为1mol。
| 阳离子 |
Na+ Mg2+ Fe3+ Al3+ Fe2+ |
| 阴离子 |
OH- CO32- Cl- NO3- SO42 - - |
①若向溶液中加入KSCN溶液无明显变化;
②若向原溶液中加入稀盐酸,有无色气体生成,该无色气体遇空气变成红棕色,且溶液中阴离子种类不变;
请推断:
(1)原溶液中含有阳离子:;含有阴离子: ;
;
(2)向原溶液中加入足量稀盐酸发生反应的离子方程式:;
(3)若向原溶液中加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,得到的固体质量为g。
X、Y、Z三种常见的短周期元素可以形成XY2、Z2Y、XY3、Z2Y2、Z2X等化合物,已知Y的离子和Z的离子有相同的电子层结构,X离子比Y离子多一个电子层。试回答:
(1)写出X、Y、Z三种元素的符号和名称:;
(2)分析Z2Y2中含有的化学键类型:;
(3)写出Z2Y2与二氧化碳反应的方程式:;
(4)用电子式表示X和Z两元素形成化合物的过程:。
在第三周期元素及其单质和化合物中,原子半径最小的元素是________;氧化性最强的单质是________,还原性最强的单质是________;金属的熔沸点最低的单质是________;最高价氧化物对应水化物中,最强的酸是________,最强的碱是_______;形成的两性化合物有________、________。