下列反应的离子方程式中正确的是
| A.实验室用浓盐酸与MnO2反应制Cl2:MnO2+2H++2Cl—====Cl2↑+Mn2++H2O |
| B.小苏打溶液中加入少量的石灰水:Ca2++2OH—+2HCO3—===CaCO3+CO32—+2H2O |
| C.往Ca(ClO)2溶液中通入少量的SO2:Ca2++2ClO—+SO2+H2O=2HClO+CaSO3↓ |
| D.碳酸氢钙溶液加到醋酸中:Ca(HCO3)2+2CH3COOH=Ca2++2CH3COO—+2CO2↑+2H2O |
化学与社会、生产、生活紧切相关。下列说法正确的是
| A.棉花和木材的主要成分都是纤维素,蚕丝和人造丝的主要成分都是蛋白质 |
| B.石油干馏可得到石油气、汽油、煤油、柴油等 |
| C.变质的油脂有特殊难闻气味,是因为油脂发生了氧化反应 |
| D.制作快餐盒的聚苯乙烯塑料是易降解塑料 |
某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。下列说法正确的是
| A.正极反应为AgCl +e-=Ag +Cl- |
| B.放电时,交换膜右侧溶液中有大量白色沉淀生成 |
| C.若用NaCl溶液代替盐酸,则电池总反应随之改变 |
| D.当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子 |
磷酸燃料电池是目前较为成熟的燃料电池之一,其基本组成及反应原理如下图所示。下列说法不正确的是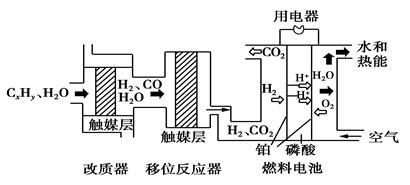
| A.该系统中不只存在化学能和电能的相互转化 |
B.在移位反应器中,反应CO(g)+H2O(g)  CO2(g)+H2(g)(ΔH>0),若温度越高,则v(CO)越大 CO2(g)+H2(g)(ΔH>0),若温度越高,则v(CO)越大 |
| C.改质器和移位反应器的作用是将CxHy转化为H2和CO2 |
| D.该电池正极的电极反应为O2+4H+—4e-===2H2O |
一定条件下,可逆反应X(g)+3Y(g) 2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),平衡时X、Y、Z的浓度分别为0.1mol•L﹣1、0.3mol•L﹣1、0.08mol•L﹣1,则下列判断不正确的是
2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),平衡时X、Y、Z的浓度分别为0.1mol•L﹣1、0.3mol•L﹣1、0.08mol•L﹣1,则下列判断不正确的是
| A.c1:c2的值不能确定 |
| B.平衡时,Y和Z的生成速率之比为3:2 |
| C.0.28mol•L﹣1<c1+c2+c3<0.56mol•L﹣1 |
| D.c1的取值范围为0<c1<0.14mol•L﹣1 |
下列说法正确的是
| A.在100℃、101 kPa条件下,1 mol液态水汽化时需要吸收40.69 kJ的热量,则H2O(g)=H2O(l)的ΔH=+40.69 kJ·mol-1 |
| B.已知CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-802.33 kJ·mol-1,则CH4的燃烧热为802.33 kJ |
| C.稀硫酸与0.1 mol·L-1NaOH溶液反应的热化学方程式为:H+(aq)+OH-(aq)=H2O(l)△ H =-57.3 kJ·mol-1 |
| D.已知S(g)+O2(g)=SO2(s) ΔH1,S(g)+O2(g)===SO2(g) ΔH2,则ΔH2<ΔH1 |