(1)25℃,柠檬水的pH是3,其中c(OH-)==
(2)下列溶液中,c(H+)由小到大的排列顺序是
① 0.1mol/L HCl 溶液 ② 0.1mol/L H2SO4溶液
③ 0.1mol/L NaOH溶液 ④0.1mol/L CH3COOH溶液
(3)在25℃时,1mol· L-1的①(NH4)2SO4 ②CH3COONH4 ③(NH4)2Fe(SO4)2 ④NH4Cl的溶液中,c(NH4+)由大到小的顺序为
(4)pH=3盐酸和pH=11氨水等体积混合后溶液呈 性(选填“酸”、“中”或“碱”),溶液中c(NH4+) c(Cl-)(选填“ >”“=”“<” )。
下表为元素周期表的一部分,a、b、c…为元素周期表中前4周期的部分元素。
回答下列问题:
| a |
|||||||||||||||||
| e |
f |
g |
|||||||||||||||
| b |
hh |
||||||||||||||||
| c |
d |
[ |
d |
||||||||||||||
(1)d3+的未成对电子数为个;
(2)请比较e、f、g三种元素的第一电离能由大到小的顺序(写元素符号)
(3)请写出h元素原子价电子轨道表示式;
(4)ea3分子的电子式是,其分子的空间构型是,分子中e原子的杂化类型是。
氮是地球上极为丰富的元素。
(1)Li3N晶体中氮以N3-存在,基态N3-的核外电子排布式为。
(2)X+中所有电子正好充满K、L、M三个电子层,它与N3-形成的晶体结构如图所示。X的元素符号是,与同一个N3-相连的X+有个。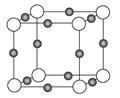
(1)A元素的负一价离子和B元素的正一价离子的电子层结构都与氩相同,A的离子结构示意图为,B元素名称为;
(2)C元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,C的元素基态原子的外围电子排布式为.
(3)D元素的原子序数为33,该元素原子的核外电子共有种不同的运动状态,此元素原子的核外电子排布式是
(4)N≡N的键能为942kJ·mol-1,N—N单键的键能为247kJ·mol-1,通过计算说明N2中的键更稳定(填“σ”或“π”)。
(5)下列4种物质熔、沸点由高到低排列为(填序号).
①金刚石②晶体锗③晶体硅④金刚砂
(12分)下表是元素周期表的一部分,所列字母分别代表一种元素: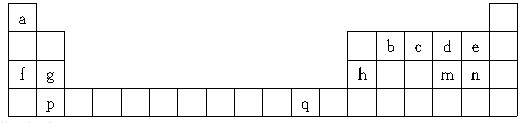
(1)q元素位于周期表中________区。
(2)下列有关说法正确的是________(填字母)。
| A.b、c、d元素的电负性逐渐增大 |
| B.f、g、h元素的第一电离能逐渐增大 |
| C.md2与bd2的化学性质类似,都是极性分子 |
| D.f、g分别与e组成的物质的晶格能,前者比后者低 |
E. a、b和d以原子个数比2∶1∶1构成的最简单化合物分子中σ键和π键的个数比为3∶1
F. ae熔沸点高于an,是因为ae分子内共价键键能大于an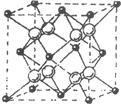
(3)mdn2是一种很重要的化学试剂,可以作为氯化剂和脱水剂。该分子的几何构型是________;中心原子采取________杂化方式。
(4)pe2晶胞如右图所示,该晶体中e-离子的配位数为________;该晶体中p2+所采用堆积方式如下图中的________(填“a”或“b”)。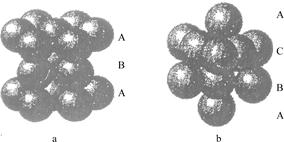
(14分)钢铁生产中的尾气易造成环境污染,清洁生产工艺可消减污染源并充分利用。已知:
① Fe2O3(s)+3CO(g) Fe(s)+3CO2(g);ΔH=-25 kJ/mol
Fe(s)+3CO2(g);ΔH=-25 kJ/mol
② 3Fe2O3(s)+CO(g) 2Fe3O4(s)+CO2(g);ΔH=-47 kJ/mol
2Fe3O4(s)+CO2(g);ΔH=-47 kJ/mol
③ Fe3O4(s)+CO(g) 3FeO(s)+CO2(g);ΔH=+17 kJ/mol
3FeO(s)+CO2(g);ΔH=+17 kJ/mol
(1) 试计算反应:FeO(s)+CO(g) Fe(s)+CO2(g)的ΔH=________。
Fe(s)+CO2(g)的ΔH=________。
(2) 已知1 092 ℃时(1)中反应的平衡常数为0.35,在1 L的密闭容器中,投入7.2 g FeO和0.1 mol CO加热到1 092 ℃并保持该温度,反应在t1时达平衡。
① t1时反应达平衡后,CO气体的体积分数为________。
② 反应(1)在一定条件下达到平衡,则下列叙述表明该反应已经达到平衡状态的是_____(填字母)。
A.混合气体的密度不变 B.CO的浓度不再改变
C.v(CO)正=v(CO2)逆 D.容器内总压强不变
(3) 含铁元素的高铁酸钾(K2FeO4)是一种优良的水处理剂。
① K2FeO4溶于水是一个可逆的过程,放出一种无色无味气体。其杀菌消毒、净化吸附水中的悬浮杂质的原理可用离子方程式表示为__________________。
② FeO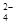 在水溶液中的存在形态如右图所示,纵坐标表示分数分布。则下列说法不正确的是________(填字母)。
在水溶液中的存在形态如右图所示,纵坐标表示分数分布。则下列说法不正确的是________(填字母)。
A.不论溶液酸碱性如何变化,铁元素都有4种存在形态
B.向pH=10的这种溶液中加硫酸至pH=2,HFeO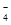 的分布分数逐渐增大
的分布分数逐渐增大
C. 向pH=6的这种溶液中加KOH溶液,发生反应的离子方程式为HFeO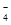 +OH-===FeO
+OH-===FeO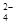 +H2O
+H2O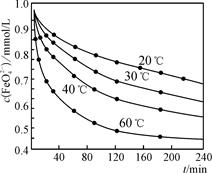
③ 高铁酸钾还可制作充电电池,原理为: 3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH
3Zn(OH)2+2Fe(OH)3+4KOH
该电池充电时阳极电极反应式为____。
④ 将适量K2FeO4溶解于pH=4.74的溶液中,配制成c(FeO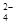 )=1.0 mmol/L的试样,将试样分别置于20 ℃、30 ℃、40 ℃和60 ℃的恒温水浴中,测定c(FeO
)=1.0 mmol/L的试样,将试样分别置于20 ℃、30 ℃、40 ℃和60 ℃的恒温水浴中,测定c(FeO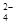 )的变化,结果见右图。该操作的目的是__________________。
)的变化,结果见右图。该操作的目的是__________________。