(14分)钢铁生产中的尾气易造成环境污染,清洁生产工艺可消减污染源并充分利用。已知:
① Fe2O3(s)+3CO(g) Fe(s)+3CO2(g);ΔH=-25 kJ/mol
Fe(s)+3CO2(g);ΔH=-25 kJ/mol
② 3Fe2O3(s)+CO(g) 2Fe3O4(s)+CO2(g);ΔH=-47 kJ/mol
2Fe3O4(s)+CO2(g);ΔH=-47 kJ/mol
③ Fe3O4(s)+CO(g) 3FeO(s)+CO2(g);ΔH=+17 kJ/mol
3FeO(s)+CO2(g);ΔH=+17 kJ/mol
(1) 试计算反应:FeO(s)+CO(g) Fe(s)+CO2(g)的ΔH=________。
Fe(s)+CO2(g)的ΔH=________。
(2) 已知1 092 ℃时(1)中反应的平衡常数为0.35,在1 L的密闭容器中,投入7.2 g FeO和0.1 mol CO加热到1 092 ℃并保持该温度,反应在t1时达平衡。
① t1时反应达平衡后,CO气体的体积分数为________。
② 反应(1)在一定条件下达到平衡,则下列叙述表明该反应已经达到平衡状态的是_____(填字母)。
A.混合气体的密度不变 B.CO的浓度不再改变
C.v(CO)正=v(CO2)逆 D.容器内总压强不变
(3) 含铁元素的高铁酸钾(K2FeO4)是一种优良的水处理剂。
① K2FeO4溶于水是一个可逆的过程,放出一种无色无味气体。其杀菌消毒、净化吸附水中的悬浮杂质的原理可用离子方程式表示为__________________。
② FeO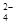 在水溶液中的存在形态如右图所示,纵坐标表示分数分布。则下列说法不正确的是________(填字母)。
在水溶液中的存在形态如右图所示,纵坐标表示分数分布。则下列说法不正确的是________(填字母)。
A.不论溶液酸碱性如何变化,铁元素都有4种存在形态
B.向pH=10的这种溶液中加硫酸至pH=2,HFeO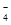 的分布分数逐渐增大
的分布分数逐渐增大
C. 向pH=6的这种溶液中加KOH溶液,发生反应的离子方程式为HFeO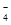 +OH-===FeO
+OH-===FeO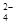 +H2O
+H2O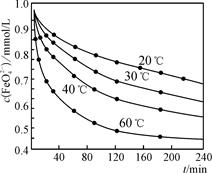
③ 高铁酸钾还可制作充电电池,原理为: 3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH
3Zn(OH)2+2Fe(OH)3+4KOH
该电池充电时阳极电极反应式为____。
④ 将适量K2FeO4溶解于pH=4.74的溶液中,配制成c(FeO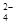 )=1.0 mmol/L的试样,将试样分别置于20 ℃、30 ℃、40 ℃和60 ℃的恒温水浴中,测定c(FeO
)=1.0 mmol/L的试样,将试样分别置于20 ℃、30 ℃、40 ℃和60 ℃的恒温水浴中,测定c(FeO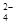 )的变化,结果见右图。该操作的目的是__________________。
)的变化,结果见右图。该操作的目的是__________________。
硝酸具有强氧化性,请分别写出Cu与浓硝酸、稀硝酸反应的化学方程式。
、。现有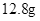 铜片与某浓度的硝酸反应,生成气体的体积在标准状况下为
铜片与某浓度的硝酸反应,生成气体的体积在标准状况下为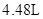 ,则被还原的硝酸的物质的量为。
,则被还原的硝酸的物质的量为。
钠及其化合物具有广泛的用途。
(1)常温下,浓度均为0.1mol·L-1的下列五种钠盐溶液的pH如下表;
| 溶质 |
CH3COONa |
NaHCO3 |
Na2CO3 |
NaClO |
NaCN |
| pH |
8.8 |
9.7 |
11.6 |
10.3 |
11.1 |
上述盐溶液中的阴离子,结合H+能力最强的是________,根据表中数据,浓度均为0.01mol·L—1的下列四种酸的溶液分别稀释100倍,pH变化最大的是________(填编号)。
A.HCN B.HClOC.CH3COOHD.H2CO3
(2)有①100ml 0.1 mol/L NaHCO3②100ml 0.1 mol/L Na2CO3两种溶液,溶液中水电离出的H+个数:
①②(填“>”、“=”或“<”,下同)。溶液中阴离子的物质的量浓度之和:①②
(3)NaHCO3是一种(填“强”或“弱”)电解质;写出HCO3―水解的离子方程式:,常温下,0.1 mol·L-1NaHCO3溶液的pH大于8,则溶液中Na+、HCO3―、H2CO3、CO32―、OH―五种微粒的浓度由大到小的顺序为:。
(4)实验室中常用NaOH来进行洗气和提纯。
①当150ml 1mol/L的NaOH溶液吸收标准状况下2.24LCO2时,所得溶液中各离子浓度由大到小的顺序为
②几种离子开始沉淀时的PH如下表:
| 离子 |
Fe2+ |
Cu2+ |
Mg2+ |
| pH |
7.6 |
5.2 |
10.4 |
当向含相同浓度Cu2+、Mg2+、Fe2+离子的溶液中滴加NaOH溶液时,(填离子符号)先沉淀,
Ksp[Fe(OH)2]Ksp[Mg(OH)2] (填“>”、“=”或“<”),要使0.2mol/L硫酸铜溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则应向溶液里加入氢氧化钠溶液使溶液pH为。(KspCu(OH)2=2×10-20mol2·L-2)
在一个1 L的密闭容器中,加入2 mol A和1 mol B,发生下列反应:
2A(g) + B(g)  3C(g) + D(s), 达到平衡时,C的浓度为1.2 mol·L-1。
3C(g) + D(s), 达到平衡时,C的浓度为1.2 mol·L-1。
(1)维持容器的温度不变,若将容器的体积缩小至一半,则平衡移动(填“向正反应方向”、“向逆反应方向”或“不”),C的浓度为mol/L,平衡常数K=。
(2)能说明该反应达到化学平衡状态的是
a.容器中气体总压强不再改变 b.容器中气体的密度不再改变
c.2V正(A)=3V逆(C) d.气体平均相对分子质量不再改变
(3)维持容器的压强和温度不变,按下列四种配比作为起始物质,达到平衡后,C的浓度仍是1.2 mol·L-1的是。
a.4 mol A + 2 mol B
b.3 mol C + 1 mol D
c.2 mol A +1 mol B + 1 molD
(4)若维持容器的体积和温度不变,反应从逆反应开始,按不同配比作为起始物质,达到平衡时,C的浓度仍是1.2 mol·L-1,则C的起始物质的量应满足的条件是。
(9分)下图是一个甲烷燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题: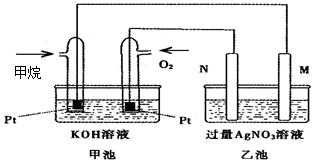
(1)N的电极反应式为 :
乙池的总化学方程式是,
加入甲烷的铂电极的电极反应式为。
(2)在此过程中,乙池中某一电极析出金属银4.32g时,甲池中理论上消耗氧气为L(标准状况下);若此时乙池溶液的体积为200mL,则乙池中溶液的H+的浓度为。
(8分)(1)向20.00mL稀氨水中逐滴加入等物质的量浓度的盐酸,请回答相关问题:
①当加入10.00mL盐酸时,溶液中各种离子浓度之间的大小关系为:
②当溶液pH=7时,反应所消耗的物质(包括还在溶液中存留的物质)之间的关系为:n(NH3·H2O)_______n(HCl),溶液中c( NH4+)_______c(Cl-)。(填“>”或“<”或“=” )
(2)室温下,如果将0.1mol NH4Cl和0.05mol NaOH全部溶于水,形成混合溶液(假设无损失),
①___和__两种粒子的物质的量之和等于0.1mol。
②___和___两种粒子的物质的量之和比OH―多0.05mol。