在电解炼铝过程中加入冰晶石(用“A”代替),可起到降低Al2O3熔点的作用。冰晶石的生产原理为2Al(OH)3+12HF+3Na2CO3=2A+3CO2↑+9H2O。根据题意完成下列填空:
(1)冰晶石的化学式为________,含有离子键、________等化学键。
(2)生成物中含有10个电子的分子是________(写分子式),该分子的空间构型为________,中心原子的杂化方式为________。
(3)反应物中电负性最大的元素为________(填元素符号),写出其原子最外层的电子排布图:________。
(4)Al单质的晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示。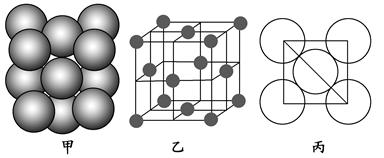
若已知Al的原子半径为d,NA代表阿伏加德罗常数,Al的相对原子质量为M,则一个晶胞中Al原子的数目为________;Al晶体的密度为________(用字母表示)。
下表为元素周期表的一部分,请回答有关问题:
| IA |
IIA |
IIIA |
IVA |
VA |
VIA |
VIIA |
0 |
|
| 2 |
① |
⑥ |
② |
|||||
| 3 |
③ |
④ |
⑤ |
⑦ |
⑧ |
|||
| 4 |
⑨ |
⑩ |
(1)画出①的原子结构示意图:, ⑩的元素名称:
(2)③④⑤原子半径由大到小的顺序是(填元素符号)
(3)表中最活泼的金属是,非金属性最强的元素是;(填写元素符号)
(4)表中能形成两性氢氧化物的元素是,写出该元素的氢氧化物与⑨的最高价氧化物对应水化物反应的离子方程式:。
(5)用电子式表示③与⑥的化合物的形成过程:。
由铜、锌和稀硫酸组成的原电池中:
(1)锌是极,电极反应式是。
(2)铜是极,电极反应式是。
(3)在铜极上可以观察到有(填实验现象)
根据下图所示回答有关问题:
(1)甲池为(选填“原电池”或“电解池”),石墨A上发生的电极反应式为:。
(2)乙池中Zn棒为极, Zn棒上发生反应的电极反应式为:。
(3)石墨B上刚好有9.6克物质析出时,则反应过程中转移的电子数为。
牛奶放置时间长了会变酸,这是因为牛奶中含有不少乳糖,在微生物的作用下乳糖分解而变成乳酸,乳酸的结构简式为 。已知有机物中若含有相同的官能团,则化学性质相似。完成下列问题:
。已知有机物中若含有相同的官能团,则化学性质相似。完成下列问题:
(1)写出乳酸分子中官能团的名称。
(2)一定条件下乳酸能发生的反应类型有______________ (填序号)。
| A.水解反应 |
| B.取代反应 |
| C.加成反应 |
| D.中和反应 |
E.氧化反应
F.酯化反应
(3)写出过量乳酸与碳酸钠溶液反应的化学方程式。
(4)乳酸在浓硫酸作用下,两分子相互反应生成链状结构的物质,写出此有机生成物的结构简式_____。
下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题: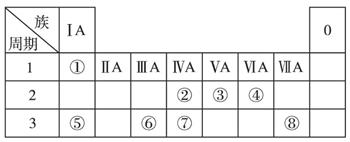
(1)在以上元素的原子中,形成化合物种类最多的是(填元素符号)。
(2)地壳中含量居于第二位的元素在周期表中的位置是。
(3)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式、。
(4)W是第五周期与④同主族的元素。据此推测W不可能具有的性质是。
| A.最高正化合价为+6价 |
| B.气态氢化物比H2S稳定 |
| C.最高价氧化物的水化物的酸性比硫酸弱 |
| D.单质在常温下可与氢气化合 |
(5)由元素⑥、⑧形成的物质X与由元素①、③形成的化合物Y可发生以下反应: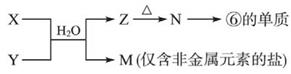
X溶液与Y溶液反应的离子方程式,M中阳离子的鉴定方法。