某化学兴趣小组进行溶液的配置和粗盐的初步提纯实验.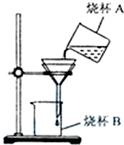
(1)配置150g质量分数为10%的氢氧化钠溶液.
①计算:需要氢氧化钠固体的质量为 g;水的体积为 mL(水的密度近似看作1g/cm3)
②称量:调节托盘天平平衡后,将 放在托盘天平的左盘,称量其质量.然后再右盘添加 .最后添加氢氧化钠固体,直至天平平衡.
③溶解:用量筒量取所需的水,倒入装有氢氧化钠固体的烧杯里,用玻璃棒 ,使其溶解,并冷却至室温.
④存储:把配好的溶液装入试剂瓶,塞好橡皮塞并 ,放到指定的地方.
(2)粗盐的初步提纯实验
①称取5.0g粗盐,用药匙逐步加入10mL水中,知道粗盐不再溶解为止.还需要进行的实验步骤的顺序为:称量剩余粗盐、 (填编号)
| A.过滤 | B.计算产率 | C.蒸发 | D.称量精盐 |
②过滤操作如图所示,指出其中的错误之处: ; ; ;
.
日常生活中的许多现象,都可以用化学知识进行解释。请你用所学化学知识,回答下列问题。
(1)衣服上的油污用汽油洗比用水洗效果更好,原因是。但若在水中加入洗涤剂,也会有很好的洗涤效果,原因是洗涤剂可以起到(填字母,下同)。
A.催化作用 B.氧化作用 C.乳化作用
(2)日常生活中,人们常把煤做成蜂窝状(右图),这样做的目的是,燃煤取暖若通风不畅,常引发煤气中毒事故,煤产生“煤气”的过程用化学方程式表示为。除排放煤气外,燃煤与多种环境污染问题有关,下列环境污染与燃煤没有直接关系的是。
A.酸雨 B.温室效应 C.臭氧层破坏 D.可吸入颗粒增加
(3)干果类食品常采用真空包装,目的是将食品与隔绝。 氮气常用作糕点包装袋内的填充气,氮气的下列性质,与该用途有关的是(填字母)。
A.无毒 B.难溶于水 C.化学性质稳定 D.密度与空气相近
(5分)在实验室常用下图装置利用一种药品制取氧气,
(1)将制取氧气的装置图补充完整
(2)写出用该装置制取氧气的化学方程式:______________________________
(3)若收集的氧气不纯,原因可能是___________________________
(3分)某工厂排放的废水中含有:CuSO4、FeSO4,为处理废水,并回收一种金属和一种晶体,在设计的方案中有如下操作,试回答: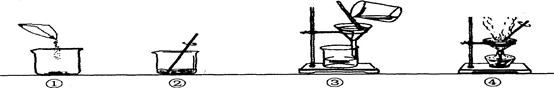
(1)上图实验中,操作③存在错误是:_______________________
(2)发生的化学反应方程式为_______________________该反应基本类型是______反应
(3分)下图是甲、乙、丙三个原子的结构模型,请通过比较归纳:
(1)在上述原子中,画出“甲”的原子结构示意图是______
(2)甲、乙、丙都属于______元素。
(1)用熟石灰改良土壤的酸性.熟石灰的化学式为____
(2)用洗涤剂洗碗,洗涤剂所起的作用是______作用
(3)早餐吃一个鸡蛋喝一杯牛奶,为人体提供的营养素是_________
(4)黑龙江盛产大豆,该植物无需施加的化肥是_______