在除杂质的实验操作中,为了将溶液中的杂质完全去除,通常需 加入过
加入过 量的除杂质试剂。某校化学课外活动小组为了除去粗盐中含有少量Na2SO4、MgCl2,设计了下列实验步骤:
量的除杂质试剂。某校化学课外活动小组为了除去粗盐中含有少量Na2SO4、MgCl2,设计了下列实验步骤: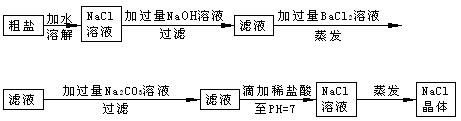
试简要说明:
(1)加入过量BaCl2的溶液的原因_______ 。
(2)判断BaCl2已过量的方法是
(3)加入过量Na2CO3的溶液的原因______ ___ _ _。
(4)滴加稀盐酸直至pH=7的目的是____ ___ __;
写出这时反应的化学方程式
现根据以下几个实验做出了下列的图象:横坐标表示向某溶液中加入另一种物质的量的变化,纵坐标表示随之引起沉淀量的变化。根据实验内容,选择相应图象的字母填空
(1) 在澄清石灰水中通入过量的CO2气体:。
(2) 在用盐酸酸化的AlCl3溶液中滴加NaOH溶液至过量。
(3) 在AlCl3溶液中逐滴加入氨水至过量。
(4) 在NaAlO2溶液中滴加HCl溶液至过量.
(5) 在NaOH溶液中逐 滴加入AlCl3溶液至过量.
滴加入AlCl3溶液至过量.
A、B、C为3种单质(其中A为固体,B、C为气体),D的溶液为棕黄色,加氢氧化钠溶液后出现红褐色沉淀,B、C反应的产物易溶于水得到无色溶液E。它们之间的转化关系如图: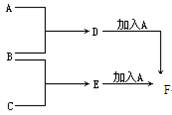
填写下列空白:物质(写化学式)A是______ B是______
C是______D 是E 是F是
下表是周期表中的一部分,根据A—I在周期表中的位置,用元素符号或化学式回答下列问题:
| 族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
| 1 |
A |
|||||||
| 2 |
C |
E |
G |
H |
J |
|||
| 3 |
B |
[] |
D |
F |
I |
(1) 在B、C、D、E、F、G、H中,原子半径最大的是。
(2) H离子的结构示意图是B和H按1∶1化合而形成的化合物的电子式是
(3) 最高价氧化物的水化物碱性最强的是,酸性最强的是;
(4)表中元素,化学性质最不活泼的是,氧化性最强的单质是;
(5)A分别与 E、F、G、H形成的化合物中,最稳定的;
(6)C的性质和D相似,写出C最高价氧化物的水化物和B最高价氧化物的水化物反应的离子反应方程式。
在FeSO4溶液中滴加入少量KSCN溶液,溶液颜色,
再滴入几滴氯水,溶液颜色,因为有生成。
实验室配制的FeCl2溶液由于各种原因很容易变质,为了防止其水解,我们经常在里面加入____;为了防止其被氧化,经常加入_____,相应的化学反应方程式为_________________。_______
将铝条进入硝酸汞溶液中,取出后用滤纸吸干,露置于空气中,看到的现象是________,其原理是(化学方程式)_________________,___________________。