某实验需要80 mL、1 mol/L的Na2CO3溶液,现通过如下操作配制:
① 称量 g Na2CO3固体放入小烧杯中,加适量蒸馏水溶解。为加快溶解可以使用 玻璃棒搅拌
②待溶液冷却到室温后,小心转入 (填仪器名称)
③继续加蒸馏水至液面至刻度线1~2cm处,改用 (填仪器名称)小心滴加蒸馏水至溶液凹液面最低点与刻度线相切
④将容量瓶塞紧,充分摇匀。
⑤用少量蒸馏水洗涤玻璃棒和烧杯2~3次,每次洗涤的溶液都转入容量瓶,并轻轻摇匀
(1)操作步骤正确的顺序是 (填序号)。
(2)使用容量瓶前必须进行的一项操作是
(3)若所配溶液的密度为1.06 g/mL,则该溶液的质量分数为 。
(4)若取出20 mL配好Na2CO3的溶液,加蒸馏水稀释成c(Na+) ="0.1" mol/L的溶液,则稀释后溶液的体积为 mL
(5)在配制Na2CO3溶液时,下列操作中的 会导致结果偏低
①用拖盘天平称量时砝码放在左盘
②将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外
③定容时俯视刻度线
④未冷却到室温就转移到容量瓶中
⑤干净的容量瓶未经干燥就用于配制溶液
下表是实验室制备气体的有关内容:
| 编号 |
实验内容 |
实验原理 |
气体发生装置 |
| ① |
制备氧气 |
H2O2→O2 |
|
| ② |
制备氨气 |
NH4Cl→NH3 |
|
| ③ |
制备氯气 |
HCl→Cl2 |
(1) 从上述气体制备原理中:从制备过程看,必须选择合适的氧化剂才能实现的是 (填气体的化学式,下同);从反应原理看,明显不同于其他两种气体的是 。
(2) 根据表中所列实验原理,从下列装置中选择合适的气体发生装置,将其编号填入上表中的空格中。
ⅠⅡ Ⅲ Ⅳ
(3) 某学习小组设计了如下图实验,将氯气依次通过下列装置以验证氯气的性质: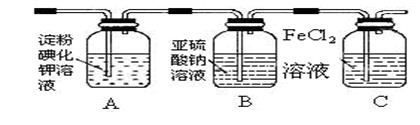
①通入氯气后,A中的现象是 ,整套实验装置存在的明显缺陷是 。
②C装置中发生反应的离子方程式为: 。
(1)用5.0mol﹒L-1的NaOH溶液配制0.1mol﹒L-1的NaOH溶液时,如图所示的仪器中,肯定不需要的是 (填序号),配制上述溶液还需要的玻璃仪器是 (填仪器名称)。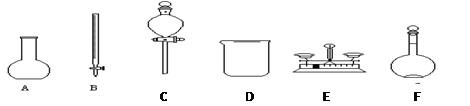
(2)在配制过程中,下列操作将导致所配溶液浓度偏低的是(填编号)



 ①准确取出的浓NaOH溶液在空气中露置时间过长;
①准确取出的浓NaOH溶液在空气中露置时间过长; ②用量器将浓NaOH溶液直接加入容量瓶,缓慢加入蒸馏水至液面最低点恰好和环形刻度线相切;
②用量器将浓NaOH溶液直接加入容量瓶,缓慢加入蒸馏水至液面最低点恰好和环形刻度线相切;
③摇匀后,液面低于刻度线,再加蒸馏水至液面最低点恰好和环形刻度线相切;
④稀释NaOH溶液的仪器未洗涤。
研究硫元素及其化合物的性质具有重要意义。
Ⅰ.利用下图装置模拟工业生产中SO2催化氧化的反应并研究SO2的性质:(熔点:SO2-76.1℃,SO3 16.8℃;沸点:SO2-10℃,SO3 45℃)
(1)甲同学按I、II、III、IV的顺序连接装置,装置II的作用是_________ ;装置III中溶液逐渐褪色,证明二氧化硫具有 性。
(2)乙同学按Ⅰ、Ⅱ、Ⅳ的顺序连接装置(装置Ⅱ中充分冷却),若装置Ⅳ中有40 mL 3.0mol/L NaOH溶液,反应后增重5.12 g,则装置Ⅳ中发生反应的化学方程式是 。
(3)某同学将足量的SO2通入一支装有氯化钡溶液的试管中,未见沉淀生成。向该试管中加入足量_____(填字母),便能产生沉淀。
| A.硫化钠溶液 | B.氨水 | C.盐酸 | D.硝酸钾溶液 |
Ⅱ.为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
称取铁钉(碳素钢)6g放入15mL浓硫酸中,加热,充分反应后得到溶液X并收集到气体Y。
(4)甲同学认为X中除Fe3+外还可能含有Fe2+。若要确认其中的Fe2+应选用________(选填序号)。
a.KSCN溶液和氯水
b.氢氧化钠溶液
c.酸性KMnO4溶液
d.铁粉和KSCN溶液
(5)乙同学取784 mL(标准状况)气体Y通入足量H2O2水溶液中,然后加入足量BaCl2溶液,经适当操作后得干燥固体4.66g。由此推知气体Y中SO2的体积百分数为________ 。(保留小数点后一位)
(6)分析上述实验中SO2体积分数的结果,丙同学认为气体Y中还可能含有H2和C02气体,产生C02的理由是_______________ (用化学方程式表示)。
氨与硝酸都是氮的重要化合物,在工农业生产中有广泛应用。
Ⅰ.实验室模拟工业氨催化氧化法制取硝酸,装置如下图所示。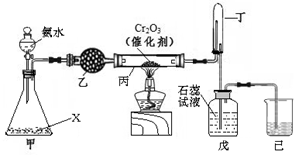
(1)若分液漏斗中氨水的浓度为9.0mol·L-1,配制该浓度的氨水100mL,用到的玻璃仪器有烧杯、玻璃棒、量筒、 、 。
(2)甲装置不需要加热即能同时产生氨气和氧气,烧瓶内固体X的化学式为 。
(3)写出受热时丙装置发生反应的化学方程式 。当戊中观察到石蕊试液变红,则说明已制得硝酸。
Ⅱ.NH3的性质
(4)氨的水溶液显弱碱性,其原因为 (用离子方程式表示),将等浓度、等体积的氨水和硝酸混合,所得溶液中离子浓度从大到小的顺序为 。
(5)已知:氨在纯氧中燃烧生成一种单质和水,利用此原理设计成氨气-氧气燃料电池。在碱性条件下,该电池的负极反应式为 。
现使用酸碱中和滴定法测定市售白醋(CH3COOH)的总酸量(g/100 mL)。
Ⅰ.实验步骤: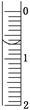
(1)量取10.00 mL食用白醋,在烧杯中用水稀释后转移到100 mL________(填仪器名称)中定容,摇匀即得待测白醋溶液。
(2)用酸式滴定管取待测白醋溶液20.00 mL于锥形瓶中,向其中滴加2滴________作指示剂。
(3)读取盛装0.100 0 mol/L NAOH溶液的碱式滴定管的初始读数。如果液面位置如图所示,则此时的读数为________mL。
(4)滴定。滴定终点的现象是__________________________________________。
Ⅱ.数据记录:
| 滴定次数 |
1 |
2 |
3 |
4 |
| V(样品) (mL) |
20.00 |
20.00 |
20.00 |
20.00 |
| V(NAOH)(消耗) (mL) |
15.95 |
15.00 |
15.05 |
14.95 |
Ⅲ.数据处理:
某同学在处理数据时计算得:
平均消耗的NAOH溶液的体积V=(15.95+15.00+15.05+14.95)/4 mL=15.24 mL。
(5)指出他的计算的不合理之处:__________________;按正确数据处理,可得市售白醋总酸量=________g/100 mL。(结果保留四位有效数字)