红磷P(s)和Cl2(g)发生反应生成 PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)。
PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)。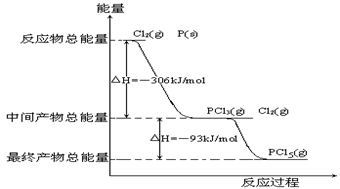
根据上图回答下列问题:
(1)P和Cl2反应生成PCl3的热化学方程式______________________________。
(2)PCl5分解成PCl3和Cl2的热化学方程式_________________ ____
(3)P和Cl2分两步反应生成1molPCl5的△H3=_________,P和Cl2一步反应生成1molPCl5的△H4______△H3(填“大于”、“小于”或“等于”)。
(12分)(1)按系统命名法命名.
①有机物CH3CH(C2H5)CH(CH3)2的名称是________________________.
②在有机物分子中若某一个碳原子连接4个不同的原子或基团,则这种碳原子称为“手性碳原子”,如: 。C7H16的同分异构体中具有“手性碳原子”的有_____种,写出其中一种的名称 _____ 。
。C7H16的同分异构体中具有“手性碳原子”的有_____种,写出其中一种的名称 _____ 。
(2)写出下列各种有机物的结构简式
①2,3-二甲基-4-乙基已烷 _____________________________________
②支链只有一个乙基且式量最小的烷烃_______________________________
③3-乙基-4-甲基-2-戊烯___________________________________________
(3)腈纶(人造羊毛)的主要成份是聚丙烯腈(丙烯腈:CH2=CH—CN),由乙炔和氢氰酸(HCN)生产聚丙烯腈所涉及的有机化学反应方程式为________________、______________,
反应所属类型分别为__________、_________。
某物质的分子式为C4H10O。
(1)它能被催化氧化生成相同碳原子数的醛有_________种,
它们对应的醇分别为(写结构简式)___________,___________。
(2)它能被催化氧化成相同碳原子数的酮有种,写出结构简式并命名_________,___________。
(3)不能被催化氧化的醇的结构简式和名称___________,___________。
(4)能发生消去反应,有机产物只有一种物质的有_________种;两种的有_________种,产物的结构简式为_________和_________。
(探究题)乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物。
完成下列各题:
(1)正四面体烷的分子式为________________,其二氯取代产物有______________种。
(2)关于乙烯基乙炔分子的说法错误的是____。
a.能使酸性KMnO4溶液褪色
b.1 mol乙烯基乙炔能与3 mol Br2发生加成反应
c.乙烯基乙炔分子内含有两种官能团
d.等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量不相同
(3)写出与环辛四烯互为同分异构体且属于芳香烃的分子的结构简式:__________________。
现有分子式都是C7H8O的芳香族化合物A、B、C三种物质。若各取少许分别滴加FeCl3溶液,只有C呈紫色;若投入金属钠,只有B无明显变化。
(1)写出A、B的结构简式______。
(2)C有多种同分异构体,若其一溴代物最多有两种,C的这种同分异构体的结构简式为________。
有机化合物A是人工合成的香料茉莉酮,其结构简式如图:
(1)该化合物中碳原子数目是_________,分子式是__________。
(2)1 mol该有机物与H2充分反应,消耗_________H2 mol。
(3)该有机物能否发生银镜反应?_____________________________。