下列变化中,属于物理变化的是
| A.氧气溶于水 | B.一氧化碳燃烧 |
| C.钠溶于水 | D.氢气燃烧 |
铜锌原电池(如图)工作时,下列叙述正确的是 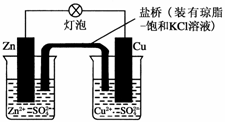
| A.正极反应为:Zn-2e-=Zn2+ |
| B.电池反应为:Zn+Cu2+=Zn2++Cu |
| C.当有1mol电子转移时,锌极减轻65g |
| D.盐桥中的K+移向ZnSO4溶液 |
下列有机分子中,所有的原子不可能处于同一平面的是
| A.CH2=CH-C≡N | B.CH2=CH-CH=CH2 |
C.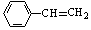 |
D.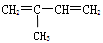 |
常温下易溶于水,在一定条件下又能与水反应的是
| A.蔗糖 | B.氯乙烷 | C.植物油 | D.葡萄糖 |
下列离子方程式中,属于水解反应的是
A.CH3COOH + H2O CH3COO- + H3O+ CH3COO- + H3O+ |
B.CO2 + H2O  HCO3- + H+ HCO3- + H+ |
C.CO32- + H2O  HCO3- + OH- HCO3- + OH- |
D.HS- + H2O  S2- + H3O+ S2- + H3O+ |
可以将五种无色液体:C2H5OH、AgNO3溶液、C2H5Br、 、KI溶液一一区分开的试剂是:
、KI溶液一一区分开的试剂是:
| A.FeCl2溶液 | B.NaOH溶液 | C.水 | D.溴水 |