下列各组中的离子,能在溶液中大量共存的是
| A.Na+ Ca2+ SO42— CO32— |
| B.Na+ Cu2+SO42— OH— |
| C.Na+H+ Cl— SO42— |
| D.Na+H+ Cl— CO32— |
用NA表示阿伏加德罗常数的值,下列叙述正确的是()
| A.24 g NaH中阴离子所含电子总数为NA |
| B.标准状况下,22.4 L苯中含有C—H键数目为6NA |
C.在碳酸钠溶液中,若c(C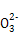 )="1" mol/L,则c(Na+)="2" mol/L )="1" mol/L,则c(Na+)="2" mol/L |
| D.通过MnO2催化使H2O2分解,产生32 g O2时转移电子数为2NA |
标准状况下,m1g气体A与m2g气体B的分子数相等,下列说法中正确的是()
A.1个A分子的质量是1个B分子的质量的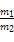 倍 倍 |
B.同温同体积的A与B的质量比为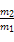 |
C.同温同质量的A与B的分子数比为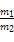 |
D.同温同压下A与B的密度比为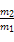 |
用NA表示阿伏加德罗常数的值,下列说法正确的是()
| A.在1 L 0.1 mol/L硫化钠溶液中阴离子总数大于0.1NA |
| B.1 mol O2作氧化剂时转移电子数一定为4NA |
| C.标准状况下,22.4 L戊烷所含分子数为NA |
| D.在1 L 1.0 mol/L NaCl溶液中含有NA个NaCl分子 |
NA表示阿伏加德罗常数的值,下列叙述正确的是()
| A.标准状况下,11.2 L四氯化碳中C—Cl键的数目为2.0NA |
| B.常温下,1 L 0.1 mol/L NH4NO3溶液中的氮原子数为0.2NA |
C.在反应:H2O2+Cl2 2HCl+O2中,每生成32 g氧气,转移的电子数 2HCl+O2中,每生成32 g氧气,转移的电子数为4NA |
| D.22.4 L由CO和C2H4组成的混合气体的质量一定为28 g |
设NA为阿伏加德罗常数的值。下列说法正确的是()
| A.常温常压下,17 g甲基(—14CH3)所含的中子数为9NA |
| B.pH=1的稀硫酸中含有的H+数为0.1NA |
| C.7.8 g过氧化钠与足量二氧化碳反应转移的电子数为0.1NA |
| D.3 mol NO2和足量H2O反应,转移NA个电子 |