已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l);△H="-57.3" kJ/mol,下列说法中正确的是 ( )
| A.浓硫酸和NaOH溶液反应,生成 l mol水时放热57.3 kJ |
| B.含l molH2SO4的稀硫酸与足量稀NaOH溶液中和后,放热为57.3 kJ |
| C.1L 0.l mol/L CH3COOH与1L 0.l mol/L NaOH溶液反应后放热为5.73 kJ |
| D.1L 0.l mol/L HNO3与 1L 0.l mol/L NaOH溶液反应后放热为 5.73 kJ |
低合金高强度钢Q460是支撑“鸟巢”的铁骨钢筋,除含有铁元素外,还含有Mn(锰)、Ti(钛)、Cr(铬)、Nb(铌)等合金元素,下列有关说法正确的是
| A.工业上利用热还原法冶炼金属Fe、Cr、Mn |
| B.Fe位于元素周期表的第四周期、第ⅧB族 |
C. TiO2、 TiO2、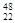 TiO2、 TiO2、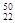 TiO2互为同位素 TiO2互为同位素 |
D.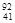 Nb3+原子核内有51个中子,核外有44个电子 Nb3+原子核内有51个中子,核外有44个电子 |
2010年诺贝尔物理奖授予发现石墨烯的开创性研究者,金刚石、石墨、C60和石墨烯的结构示意图分别如下图所示,下列说法不正确的是
| A.金刚石和石墨烯中碳原子的杂化方式不同 |
| B.金刚石、石墨、C60和石墨烯的关系:互为同素异形体 |
| C.这四种物质完全燃烧后的产物都是CO2 |
| D.石墨与C60的晶体类型相同 |
如图是一种染料敏化太阳能电池的示意图。电池的一个点极由有机光敏燃料(S)涂覆在TiO2纳米晶体表面制成,另一电极由导电玻璃镀铂构成,电池中发生的反应为: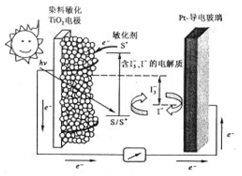
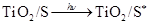 (激发态)
(激发态)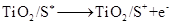
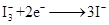
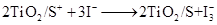
下列关于该电池叙述错误的是
| A.电池工作时,是将太阳能转化为电能 |
| B.电池中镀铂导电玻璃为正极 |
| C.电池工作时,I-离子在镀铂导电玻璃电极上放电 |
| D.电池的电解质溶液中I-和I3-的浓度不会减少 |
有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期, Z、M同主族; X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的单质晶体熔点高、硬度大,是一种重要的半导体材料。下列说法中,正确的是
| A.X、M两种元素只能形成X2M型化合物 |
| B.元素W和M的某些单质可作为水处理中的消毒剂 |
| C.元素Y的单质只能与氢氧化钠溶液反应而不能与任何酸反应 |
| D.由于W、Z、M元素的氢化物相对分子质量依次减小,所以其沸点依次降低 |
下列离子方程式表达正确的是
| A.用食醋除去水瓶中的水垢:CO32-+2CH3COOH=2CH3COO-+H2O+CO2↑ |
B.用惰性电极电解熔融氯化钠:2Cl-+2H2O Cl2↑+H2↑+OH- Cl2↑+H2↑+OH- |
| C.将氯气溶于水制备次氯酸:Cl2 + H2O=H+ + Cl- +HClO |
| D.Na2O2与H2O反应制备O2:Na2O2 + H2O= 2Na+ + 2OH- + O2↑ |