某研究性学习小组对铝热反应实验 展开研究。现行高中化学教材中对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”。查阅《化学
展开研究。现行高中化学教材中对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”。查阅《化学 手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
| 物质 |
Al |
Al2O3 |
Fe |
Fe2O3 |
| 熔点/℃ |
660 |
2054 |
1535 |
1462 |
| 沸点/℃ |
2467 |
2980 |
2750 |
- |
I. ⑴某同学推测,铝热反应所得到的熔融物应是铁铝合金。理由是:该反应放出的热量使铁熔化,而铝的熔点比铁低,此时液态的铁和铝熔合形成铁铝合金。你认为他的解释是否合理?答:_________________(填“合理”或“不合理)
⑵设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所用试是_______________。
⑶实验室溶解该熔融物,下列试剂中最好的是____________ (填序号)。
(填序号)。
A.浓硫酸 B.稀硫酸 C.稀硝酸 D.氢氧化钠溶液
II.实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。某同学取一定量上述的熔融物与一定量很稀的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴加入4mol·L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。试回答下列问题:
⑴图中OC段没有沉淀生成,此阶段发生反应的化学方程式为__________________________________。
⑵在DE段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式是
_______________ _______;
上述现象说明溶液中________ _________结合OH-的能力比_______强(填离子符号)。
(3) B与A的差值为_________mol。B点 对应的沉淀的物质的量为________mol,C点对应的氢氧化钠溶液的体积为___________mL
对应的沉淀的物质的量为________mol,C点对应的氢氧化钠溶液的体积为___________mL
一种无色透明溶液中,可能含有下列离子:K+、Mg2+、Al3+、Fe2+、Ba2+、NO3-、SO42-、HSO3-、HCO3-、I-和Cl-,取该溶液进行如下实验:
①将溶液滴在pH试纸上,呈红色。
②将少许溶液浓缩后加入铜片和硫酸,有无色气体析出,此气体通空气则立即变成红棕色。
③取少许溶液滴入BaCl2试液,则产生白色沉淀。
④取实验③中的澄清溶液,滴入AgNO3试液,产生不溶于稀HNO3的白色沉淀。
⑤另取少许溶液,滴入NaOH溶液,有白色沉淀生成,当NaOH过量时,又有部分白色沉淀溶解。
根据以上现象判断,原溶液中肯定不存在的离子是;肯定存在的离子是;不能作出判断的离子是。
“温室效应”是全球关注的环境问题之一,科学家们一直致力于CO2的“组合转化”技术研究。例如将CO2和H2以1:4或1:3的比例混合,在适当条件下反应,生成H2O的同时可分别获得重要的气态能源物质A和对植物生长有调节作用的有机物B。请回答下列问题:(1)写出生成A的化学方程式:(不必写反应条件)
(2)某小组做了如下三组对照实验来证实有机物B对植物生长的调节作用。
实验I:集气瓶中放青色、未熟的水果,在空气中盖上玻璃片。
实验II: 集气瓶中放青色、未熟的水果,通入一定量的有机物B.
实验III:集气瓶中放青色、未熟的水果,瓶底放少量KMnO4 固体。
该三组实验中,水果成熟的先后顺序为(填写实验序号)。
(3)A分子的空间构型为,B分子中有个原子共面。
(4)试推测丙烯(CH2=CH-CH3)的结构或性质,下列说法中不正确的是(填字母)
a.丙烯分子中三个碳原子在同一直线上
b.丙烯可使酸性高锰酸钾溶液褪色
c.丙烯可使溴水褪色
d.丙烯能发生加成反应。
现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下转化关系(图中有些反应的产物和反应的条件没有全部标出)。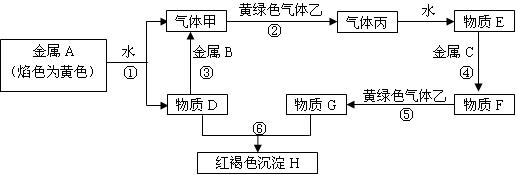
请根据图中信息回答下列问题:
(1)写出下列物质的化学式:B ________、C________、H _________、丙__________
(2)写出下列反应离子方程式:
反应①____________________反应③__________________________
(3)反应⑤属于下列反应类型中_______________(填写序号)。
A.氧化还原反应 B.分解反应 C.化合反应 D.复分解反应
将纯锌片和纯铜片按图方式插入100 mL相同浓度的稀硫酸中一段时间,回答下列问题:
(1)下列说法正确的是____________。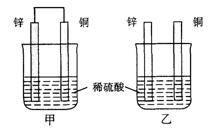
| A.甲、乙均为化学能转变为电能的装置 |
| B.乙中铜片上没有明显变化 |
| C.甲中铜片质量减少、乙中锌片质量减少 |
| D.两烧杯中溶液的pH均增大 |
(2)在相同时间内,两烧杯中产生气泡的速度:甲____乙(填“>”、“<“或“=”)。
(3)当甲中产生1.12L(标准状况)气体时,通过导线的电子数目为_______________。
(4)当乙中产生1.12L(标准状况)气体时,将锌、铜片取出,再将烧杯中的溶液稀释至1 L,测得溶液中c(H+)=0.1 mol·L-1(设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为_________________。
已知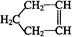 可简写为
可简写为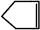 。降冰片烯的分子结构可表示为:
。降冰片烯的分子结构可表示为: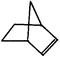
(1)降冰片烯的分子式为__________。
(2)降冰片烯的一种同分异构体(含有一个六元环的单环化合物)的结构简式为__________。
(3)有关降冰片的说法不正确的是__________。
A能溶于水 B能发生氧化反应
C能发生加成反应 D常温常压下为气体