把氯气通入稀氨水中,NH3分子上的一个H被Cl取代生成氯氨,然后加入过量的氨和氯氨作用,得到 联氨(N2H4)。
联氨(N2H4)。
(1)写出上述反应的化学方程式:________ __________
(2)联氨是一种可燃性液体,可用作火箭燃料。已知32.0g N2H4和H2O2反应生成氮气和水(气态),放出热量642kJ,该反应的热化学方程式是:
____________________________________________
(3)联氨的水溶液显弱碱性,用离子方程式表示其显弱碱性的原因:
_______________________________________________
(4)联氨—空气燃料电池是一种碱性燃料电池,电解质溶液是20%—30%的KOH溶液。联氨—空气燃料电池放电生成N2和H2O,其电极反应式是:正极________________________;负极_____________________。
X、Y、Z、W是四种常见的短周期主族元素,核电荷数依次增大。X的原子序数、元素所在周期数、族序数相同。Y、Z是同周期相邻元素,Y的最简单氢化物常用作致冷剂,Z可以形成两种液态氢化物,其中一种氢化物分子呈V型结构,其沸点远高于同族其它稳定的氢化物,Z的另一种氢化物M是常用的绿色氧化剂,分子中两种元素的原子个数比为1︰1;W的钠盐是日常生活的调味品,也是制取纯碱的原料。请回答下列问题:
(1)W形成的简单离子的原子结构示意图是____________;X、Y、Z两种元素的第一电离能的大小比较是__________________。
(2)写出X、Y两种元素形成的离子化合物的电子式______________,该化合物与水混合加热反应会产生两种气体,该反应的方程式是:_________________X、Z、W三种元素形成的化合物的结构式是____________;
(3)Y的最简单氢化物与最高价氧化物对应的水化物形成的盐R,R是一种常见的化肥和炸药,R可以促进水的电离,水溶液显_______性(填“酸”或“碱”),溶液中各种离子浓度的大小顺序是_________________;
(4)XYZ3溶液有强氧化性,写出①铜与XYZ3浓溶液反应的离子方程式________________。
②Z2溶液与适量SO2反应的离子方程式______________________________。
(5)由Y、W两种元素组成的一种化合物Q分子中,每个原子最外层均达到8电子稳定结构,该物质在工业生产中被用于面粉的漂白和杀菌,写出Q与水初步反应的化学方程式:__________________。
(选做)【化学—选修5:有机化学基础】
没食子酸丙酯简称PG,结构简式为  ,是白色粉末,难溶于水,微溶于棉子油等油脂,是常用的食用油抗氧化剂。
,是白色粉末,难溶于水,微溶于棉子油等油脂,是常用的食用油抗氧化剂。
(1)PG的分子式为 ,请写出PG分子中所含官能团的名称 ,1molPG与足量氢氧化钠溶液完全反应时,消耗的氢氧化钠的物质的量是 。
PG可发生如下转化: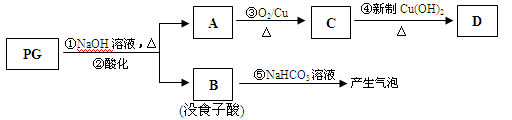
(2)A的结构简式为 ,1mol没食子酸最多可与 mol H2加成。
(3)上图的有关变化中,属于氧化反应的有(填序号) 。
(4)从分子结构或性质上看,PG具有抗氧化作用的主要原因是(填序号) 。
| A.含有苯环 | B.含有羧基 | C.含有酚羟基 | D.微溶于食用油 |
(5)反应④的化学方程式为:
(6)B有多种同分异构体,写出其中符合下列要求的同分异构体的结构简式:
i.含有苯环,且苯环上的一溴代物只有一种;ii.既能发生银镜反应,又能发生水解反应。
(选做)[化学——选修3:物质结构与性质]
血红素中含有C、O、N、Fe五种元素。回答下列问题:
(1)C、N、O、H四种元素中电负性最小的是 (填元素符合),写出基态Fe原子的核外电子排布式 。
(2)下图所示为血红蛋白和肌红蛋白的活性部分――血红素的结构式。
血红素中N原子的杂化方式有 ,在下图的方框内用“→”标出Fe2+的配位键。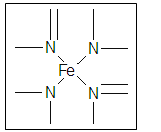
(3)NiO、FeO的晶体结构类型均与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69 pm和78 pm,则熔点NiO ________ FeO(填“<”或“>”);
(4)N与H形成的化合物肼(N2H4)可用作火箭燃料,燃烧时发生的反应是:
2N2H4(l)+ N2O4(l)=3N2(g)+ 4H2O(g)△H=-1038.7kJ/mol
若该反应中有4mol N—H键断裂,则形成的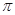 键有___________mol。
键有___________mol。
(5)根据等电子原理,写出CN—的电子式 ,1 mol O22+中含有的π键数目为 。
(6)铁有δ、γ、α三种同素异形体如下图所示。则γ晶体晶胞中所含有的铁原子数为 ,δ、α两种晶胞中铁原子的配位数之比为 。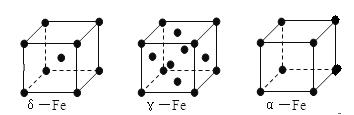
(16分)氧化铁在工业上具有广泛的应用。
I.据报道,一定条件下利用FeO2与甲烷反应可制取“纳米级”的金属铁。其反应如下:
Fe2O3(s)+3CH4(g)=2Fe(s)+3CO(g)+6H2(g)△H>0
(1)若反应在2L的密闭容器中进行,5min后达到平衡,测得反应生成Fe的质量为l.12g。则该段时间内CH4的平均反应速率为 ________________。
(2)反应达到平衡后,保持其他条件不变,仅改变某一相关元素,下列说法正确的是___(选填序号)。
a.若加入催化剂,v正增大,平衡向右移动
b.若温度升高,平衡常数K减小
c.若增大Fe2O3的量,平衡向右移动
d.若从反应体系中移走部分CO,可提高CH4的转化率
Ⅱ.工业上利用硫铁矿烧渣(主要成分为Fe2O3、A12O3、SiO2等)为原料提取Fe2O3,工艺流程如下:试回答下列问题: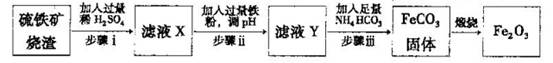
(3)步骤i烧渣中A12O3溶解的离子方程式为________________。
(4)步骤i、ⅱ、ⅲ都要进行的操作名称是__________________。
(5)结合下图,判断步骤ⅱ中调节溶液的pH不高于_________________。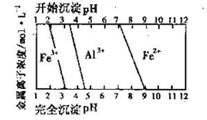
(6)已知
| 微粒平衡 |
平衡常数 |
FeCO3(s) Fe2+(aq)+CO32-(aq) Fe2+(aq)+CO32-(aq) |
Ksp=3.2×10-11 |
H2CO3 H++HCO3- H++HCO3- |
Ka1=4.36×10-7 |
HCO3- H++CO32- H++CO32- |
Ka2=4.68×10-11 |
2HCO3- H2CO3+CO32- H2CO3+CO32- |
K=1.3×10-4 |
计算反应Fe2+(aq)+2HCO3-(aq) FeCO3(s)+H2CO3(aq)的平衡常数为_______。
FeCO3(s)+H2CO3(aq)的平衡常数为_______。
(7)在空气中煅烧FeCO3生成氧化铁的化学方程式为____________。
(8)结合所学化学知识,请你设计在实验室里从上述的硫铁矿烧渣中提取氧化铁的另一种简单方案。
PET学名聚对苯二甲酸乙二醇酯( )具有优良的特性(耐热性、强韧性、电绝缘性、安全性等),且价格便宜,广泛用作纤维、薄膜、工程塑料、聚酯瓶等,某科研小组利用以下流程合成流程PET(部分试剂和反应条件略去)。
)具有优良的特性(耐热性、强韧性、电绝缘性、安全性等),且价格便宜,广泛用作纤维、薄膜、工程塑料、聚酯瓶等,某科研小组利用以下流程合成流程PET(部分试剂和反应条件略去)。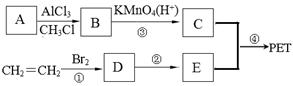
已知:
①在相同条件下芳香烃A的蒸汽密度是氢气密度的46倍;
②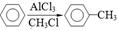 ;
;
回答下列问题:
(1)A的结构简式为___________;B的系统命名为____________;E中含有的官能团名称是______。
(2)写出反应④的化学方程式并注明反应类型:______________,____________;
(3)利用已知信息②完善下列方程式: 。
。
(4)下列有关说法正确的是_________;
a.D能能发生消去反应、取代反应
b.E可用于配制化妆品
c.乙烯分子中σ键和π键的个数之比是2:1
d.检验D中官能团的方法是加碱液并加热,用硝酸酸化后,再加入硝酸银溶液
(5)写出满足下列条件的C的所有同分异构体______________________________________。
①分子中有苯环但无其它环状结构;②能在酸或碱溶液中水解;
③1mol分子最多可与4mol NaOH反应。