中学课本中常见的几种气体:①O2②H2③CO2④Cl2⑤H2S ⑥SO2⑦NH3都要求掌握其实验室制法。根据所学知识回答有关问题(填气体编号)
(1)能用启普发生器制备的气体有 。
(2)能用浓H2SO4干燥的气体有 。
(3)能用碱石灰干燥的气体有 。
(4)收集气体的方法常有:排水法、向上排空气法和向下排空气法。如下图,用仪器A、B和橡胶管组成装置收集NO气体(①仪器A已经气密性检查;②除水外,不能选用其它试剂)正确的操作步骤是 。
铁矿石是工业炼铁的主要原料之一,其主要成分为铁的氧化物(设杂质中不含铁元素和氧元素,且杂质不与H2SO4反应)。某研究性学习小组对某铁矿石中铁的氧化物的化学式进行探究。
Ⅰ.铁矿石中含氧量的测定
①按上图组装仪器,检查装置的气密性;
②将5.0g铁矿石放入硬质玻璃管中,装置B、C中的药品如图所示(夹持仪器均省略);
③从左端导气管口处不断地通入H2,待C装置出口处H2验纯后,再点燃A处酒精灯
④充分反应后,撤掉酒精灯,再持续通入氢气至完全冷却。
(1)装置C的作用为。
(2)测的反应后装置B增重1.35g,则铁矿石中氧的百分含量为。
Ⅱ.铁矿石中含铁量的测定
(1)步骤④中煮沸的作用是。
(2)步骤⑤中用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、。
(3)下列有关步骤⑥的操作中说法正确的是。
a.因为碘水为黄色,所以滴定过程中不需加指示剂
b.滴定过程中可利用淀粉溶液作指示剂
c.滴定管用蒸馏水洗涤后可直接装液
d.锥形瓶不需要用待测液润洗
e.滴定过程中,眼睛注视滴定管中液面变化
f.滴定结束后,30s内溶液不恢复原来的颜色再读数
(4)若滴定过程中消耗0.5000mol·L−1KI溶液20.00mL,则矿石中铁的百分含量为。若省去步骤④,则所测铁的百分含量将。(偏大,偏小或无影响)
Ⅲ.由Ⅰ、Ⅱ可以推算出该铁矿石中铁的氧化物的化学式为。
下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。
(1)装置A是氯气的发生装置,其中盛放浓盐酸的仪器名称是____________,请写出该反应相应的化学方程式:。
(2)装置B中饱和食盐水的作用是;同时装置B也是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ处依次放入物质的组合应是(填字母编号)。
| 编号 |
Ⅰ |
Ⅱ |
Ⅲ |
| a |
干燥的有色布条 |
碱石灰 |
湿润的有色布条 |
| b |
干燥的有色布条 |
无水硫酸铜 |
湿润的有色布条 |
| c |
湿润的有色布条 |
浓硫酸 |
干燥的有色布条 |
| d |
湿润的有色布条 |
无水氯化钙 |
干燥的有色布条 |
(4)设计装置D、E的目的是比较氯、溴、碘单质的氧化性。反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是,该现象(填“能”或“不能”)说明溴单质的氧化性强于碘,原因是。
(5)装置F的作用是,其烧杯中的溶液不能选用下列中的(填字母编号)。
a.饱和NaOH溶液 b.饱和Ca(OH)2溶液
c.饱和Na2SO3溶液 d.饱和Na2CO3溶液[来
某研究性学习小组用下列装置(铁架台等支撑仪器略)探究氧化铁与乙醇的反应,并检验反应产物。
(1)为快速得到乙醇气体,可采取的方法是;
若实验时小试管中的溶液已经开始发生倒吸,你采取的措施是 _________(填写编号);
a.取下小试管b.移去酒精灯
c.将导管从乳胶管中取下d.以上都可以
(2)盛Cu(OH)2悬浊液的试管中可能出现的现象为___________________。
(3)如图实验,观察到红色的Fe2O3全部变为黑色固体(M),充分反应后停止加热。为了检验M的组成,进行下列实验。
①M能被磁铁吸引;加入足量稀硫酸,振荡,固体全部溶解,未观察到有气体生成;
②经检验溶液中有Fe2+和Fe3+;关于M 中铁元素价态的判断正确的是(填写编号)。
a.一定有+3价和+2价铁,一定无0价铁
b.一定有+3价、+2价和0价铁
c.一定有+3价和0价铁,一定无+2价铁
d.一定有+3和+2价铁,可能有0价铁
(4)若M的成份可表达为FexOy,用CO还原法定量测定其化学组成。称取agM样品进行定量测定,实验装置和步骤如下:
①组装仪器;②点燃酒精灯;③加入试剂;④打开分液漏斗活塞;⑤检查气密性;⑥停止加热;⑦关闭分液漏斗活塞;⑧……。正确的操作顺序是__________(填写编号)
a.①⑤④③②⑥⑦⑧b.①③⑤④②⑦⑥⑧
c.①⑤③④②⑥⑦⑧d.①③⑤②④⑥⑦⑧
(5)若实验中每步反应都进行完全,反应后M样品质量减小bg,则FexOy中=_____。
黄铁矿是工业上制取硫酸的主要原料,其主要成分为FeS2,含少量杂质(杂质不含S元素,且高温下不反应)。某化学兴趣小组用下列装置测定黄铁矿中硫元素的质量分数。
称取2.0g研细的黄铁矿样品,将样品放入石英管中,缓慢鼓入空气,再加热石英管至800~850℃;锥形瓶中盛装100 mL 0.2mol/L酸性KMnO4溶液用于吸收SO2(忽略SO2、H2SO3与氧气反应);反应结束后,每次从锥形瓶中取出25.00 mL溶液,用0.23mol/L标准H2C2O4溶液滴定,重复三次。
已知:4FeS2+11O2 2Fe2O3+8SO2;
2Fe2O3+8SO2;
2KMnO4+5SO2+2H2O K2SO4+2MnSO4+2H2SO4
K2SO4+2MnSO4+2H2SO4
请回答下列问题:
(1)连接好装置,检查装置气密性的操作是。
(2)通入空气的作用是。
(3)若实验过程中鼓入空气的速率过快,则测得的硫元素的质量分数(填“偏高”、“偏低”或“不变”)。
(4)滴定时,应选择图中的(填字母序号)盛装标准H2C2O4溶液,根据现象来判断滴定已经达到终点。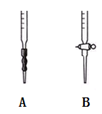
(5)滴定过程中发生反应的离子方程式是。
(6)如果黄铁矿中的硫全部转化为SO2,且被酸性KMnO4溶液完全吸收,滴定操作中,平均耗用0.23mol/L标准H2C2O4溶液21.73mL,则黄铁矿样品中硫元素的质量分数是(保留到小数点后1位)。
某兴趣小组欲利用下列装置探究A反应中Cl2的产生速率。
(1)完善A中反应:KmnO4+HCl MnCl2+Cl2 ↑+_KCl+__
MnCl2+Cl2 ↑+_KCl+__
A、B、C装置的接口连接顺序为:①→→→→(填数字序号)。
(2)当黄绿色气体缓慢进入C时,一段时间后C中溶液才变蓝。C中溶液变蓝前发生反应的离子方程式为______;少量淀粉KI溶液的作用是。
(3)若实验测得速率值偏小,小组同学作如下实验改进和反思,请帮助完成。
I用D装置代替C装置,目的是;
Ⅱ导致测得值偏小的原因可能还有:
①Cl2扩散需要一段时间
②____(任答一点)。
(4)进一步探究:仅将A装置做如图改变。则此改进欲探究的是。