(6分)物质都是由微粒构成的,请用微粒的知识回答下列问题:
⑴用化学符号和数字表示:
2个碳原子___________________; 人体中含量最多的元素________。
⑵构成物质的基本微粒有分子、原子、_________。水是由 构成的。
⑶下表为元素周期表中某一周期(同一横行)元素的原子结构示意图。
请回答下列问题: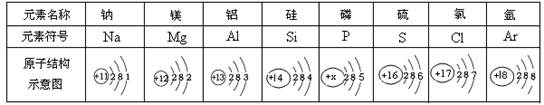
②下列说法不正确的是____________
| A.不同元素原子的核内质子数不同 |
| B.同一周期(同一横行)原子的电子层数相同 |
| C.铝原子易失去3个电子而形成带三个单位负电荷的铝离子 |
| D.同一周期(同一横行)从左向右,最外层电子数依次增大 |
请你和同学们一起完成下列实验。
(1)用浓盐酸(溶质质量分数为37%,密度为1.18
)配制200
10%稀盐酸。
①配制的主要步骤为:计算、、溶解。
②设需浓盐酸的体积为
,请列出
的计算式(不必算出结果)。
③现提供下图仪器,仪器
的名称为;配制过程中还需要的仪器有。
(2)现提供下列装置: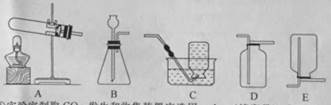
①实验室制取二氧化碳,发生和收集装置应选用(填序号),发生反应的化学方程式为。实验结束,从反应残留物中提取固体溶质时,按如下流程操作:
②如选用另一发生装置制取某种气体,发生反应的化学方程式为。
人类的生存、发展离不开化学。
(1)化石燃料是(填"可再生"或"不可再生")能源。干电池能量转化效率高,他是一种将能转化为电能的装置,太阳能热水器运行成本低,能实现(填"光-电"或"光-热")转换。
(2)人体中化学元素含量的多少直接影响人体健康。人体含量最高的元素是(填元素符号),食用加碘食盐可预防(填"A"或"B")。
A.贫血B.甲状腺疾病
(3)蒸馒头、炸油条等要用到纯碱。纯碱中含有的阴离子是(填离子符号);纯碱溶液的pH7(填">"、"="或"<")。
(4)氧化铝中铝元素的化合价是,以氧化铝等为原料生产一种耐高温、高强度陶瓷时,发生如下反应:
,其中X的化学式是。
某兴趣小组同学将CO2分别通入澄清石灰水和氢氧化钠溶液中,观察到前者变浑浊,后者无明显现象。
(1)写出上述澄清石灰水变浑浊的化学方程式。
(2)为探究CO2和NaOH是否发生了化学反应,王强设计了如图所示的A、B实验,验证CO2与NaOH溶液发生了化学反应。
实验现象为:A中试管内液面上升;B中气球胀大。
①王强认为上述实验是可行的,其共同原理是。
②李莉提出质疑,她认为上述实验不严谨,其理由是。要得到科学严谨的结论,仍利用该装置,补做的对比实验是。
③杨红通过检验生成物:向B实验后的溶液中加入,观察到有气泡产生,从而也证明CO2与NaOH发生了反应。
④你认为两实验中存在安全隐患的是(填代号),理由是 。
请根据下列装置,回答问题:
(1)写出标号①的仪器名称:。
(2)实验室用装置A制取氧气的化学方程式为。
(3)对用氯酸钾和二氧化锰的混合物制取O2后的固体残渣(假定已完全反应),通过以下四步实验操作可回收二氧化锰。正确操作的先后顺序是(填写选项序号)。
a.烘干 b.溶解 c.过滤 d.洗涤
(4)用装置F制取气体,在反应过程中,关闭活塞,过一会儿反应就会停止。其原因是。
金属材料与我们的生活息息相关。
(1)下列用品所使用的主要材料,属于金属材料的是;
(2)人们大量使用的是合金而不是纯金属,这是因为合金具有更多优良性能,例如钢比纯铁硬度(填“大”或“小”)。
(3)目前世界上已有50%以上的废钢铁得到回收利用,其目的是。
A.节约金属资源B.合理开采矿物 C.防止钢铁生锈.
(4)铜与另一种金属M的混合物(M可能是Al、Fe或Ag),在该混合物中加入足量的稀硫酸有气泡产生,则M不可能是,待反应完成后(填实验操作方法),得到铜和滤液,在滤液中加入锌片,其表面有一层黑色物质,则M是。取一定量的原混合物投入到一定量的AgNO3溶液中,充分反应后,对反应所得溶液和固体推断正确的是。
A.溶液中一定有M的离子 B.固体中一定有Ag和Cu
C.固体中一定有Ag D.溶液中一定有Ag+