实验室以食盐、二氧化碳、氨气为原料模拟生产纯碱,该实验先制得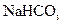 ,进而制取纯碱。主要装置如下:
,进而制取纯碱。主要装置如下: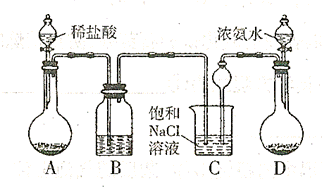
请回答下列问题:
(1)A中发生反应的离子方程式为 ;B中所盛的溶液为
。
(2)D装置用来产生 ,则固体D可以是(只填一种 ;C装置中球形漏斗的作用是 。
,则固体D可以是(只填一种 ;C装置中球形漏斗的作用是 。
(3)向C中通人气体时,应先通 ,理由是
。C中反应的总的化学方程式为
。
(4)C中分离出的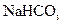 晶体可能含有的杂质有 ,用该
晶体可能含有的杂质有 ,用该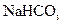 晶体制取纯碱时,有的杂质不会影响纯碱的纯度。原因是
晶体制取纯碱时,有的杂质不会影响纯碱的纯度。原因是
(用化学方程表示)。
(5)写出用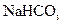 制取纯碱的化学方程式 。
制取纯碱的化学方程式 。
哈伯因为氨气的合成曾获1918年诺贝尔奖。
(1)写出实验室由氯化铵和熟石灰加热制取氨气的化学方程式:。检验氨气已装满的方法是:用_____________试纸靠近集气瓶口,现象为_________________。
(2)用图装置进行喷泉实验, 若加入酚酞,得到红色喷泉,若要得到蓝色喷泉呢,应加入酸碱指示剂。
(3)完成氨催化氧化生成为NO的反应方程式,4NH3+O2="==4NO" + 6,产物NO能在通常状况下被空气氧化为NO2,请完成下列反应生成硝酸的化学方程式:
4NO+O2+2H2O="==" 4HNO3
NO2+O2 +H2O="==" 4HNO3
(4)1.28 gCu与足量的浓硝酸反应生成的气体与一定量的O2混合,然后通入水中恰好完全反应无气体剩余,则该氧气的物质的量为mol.
(1)工业上生产玻璃、水泥都要用到的原料是。(选填石灰石、粘土、石英、石膏)
(2)漂白粉由氯气和石灰乳反应生成,其有效成分是。(填化学式)
(3)测定硅铁合金中硅的含量可以有两种方法,其一是将合金粉末加入足量的稀硫酸中,其二是将合金粉末加入足量的中,都可以通过收集生成气体并测定其体积数据而确定硅含量。写出第二种方法的反应离子方程式。
选用一种试剂除去下列物质中的杂质(括号中为杂质),并写出其化学方程式或离子方程式。可供选用的试剂:
| A.氢氧化钠溶液 | B.水 | C.二氧化碳气体 | D.铁粉E铜粉,(题中填入试剂代号) |
(1)Na2CO3 (Na2O2) 除杂剂,化学方程式;
(2)FeCl2溶液(FeCl3) 除杂剂,离子方程式;
(3)Fe粉(Al粉) 除杂剂,离子方程式;
(4)NO(NO2)除杂剂___________,化学方程式__________________________________。
标准状况下,有氧气和氯气组成的混合气体共500mL。通入氢气,一定条件下使它们恰好完全反应,然后加水得到250mL盐酸溶液。从中取出25mL,用25mL 0.08mol·L-1 NaOH溶液恰好中和。则
(1)盐酸溶液的物质的量浓度mol·L-1。
(2)氢气的体积为mL。
a、b、c、d、e是含有一种相同元素的五种物质,可发生如下转化: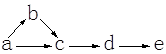
其中: a是单质;b是气体;c、d是氧化物;e是含氧酸。
(1)如果a是一种淡黄色粉末固体,试推断这五种物质(用化学式表示):
a;b;c;d;e。
(2)如果a是一种常见气体,试推断这五种物质(用化学式表示):
a;b;c;d;e。