等质量的SO2和SO3分子数之比为 ,氧元素质量之比为 。同质量的氨气和硫化氢气体中所含氢原子个数比是 ,若两者所含氢原子个数相等,它们的物质的量比是 。
(I)按官能团的不同,可以对有机物进行分类,请指出下列有机物的种类,填在横线上。
(1CH3CH=CHCH3 ;
(2)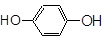 ;
;
(3) ;
;
(4) ;
;
(5)CH2BrCH2CH2CH2Br。
(II)乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物(如图所示)。
完成下列各题:
(1)正四面体烷的分子式为____________,其二氯取代产物有________种。
(2)关于乙烯基乙炔分子的说法错误的是____________。
a.能使KMnO4酸性溶液褪色
b.1摩尔乙烯基乙炔能与3摩尔Br2发生加成反应
c.乙烯基乙炔分子内含有两种官能团
d.等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量不相同
(3)写出与环辛四烯互为同分异构体且属于芳香烃的分子的结构简式:_________。
烯丙醇是一种无色有刺激性气味的液体,是重要的有机合成原料,其结构简式为CH2=CH—CH2OH。请回答:
(1)烯丙醇的分子式为;烯丙醇中除碳碳双键外还含有官能团的是。
(2)0.3mol 烯丙醇与足量金属钠反应,能生成标准状况下的氢气L。
(3)写出烯丙醇与溴水反应的化学方程式,
(4)烯丙醇与CH3CO18OH发生酯化反应的化方程式为,酯化反应生成的产物在一定条件下可以发生加聚反应得到高分子化合物,其结构简式为。
某人设计淀粉利用方案如图所示:其中:A能催熟水果,B是高分子化合物,D是有水果香味的物质。请回答以下问题:
(1)C6H12O6的名称是_____,A的电子式为_______,C中含有官能团名称;
(2)A→B反应类型_____________;C→D反应类型_________________
(3)写出下列转化的化学方程式:
①A→B:,
②C→D:,
③CH3CH2OH→CH3CHO:。
下表是元素周期表的一部分,请回答有关问题: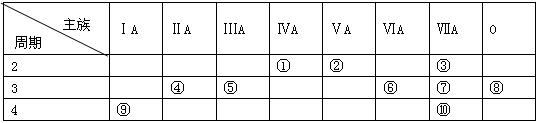
(1)表中化学性质最不活泼的元素,其原子结构示意图为 ;
(2)表中能形成两性氢氧化物的元素是 (用元素符号表示),写出该元素的单质与⑨最高价氧化物的水化物反应的离子方程式为;
(3)②、⑥、⑦三种元素的最高价氧化物的水化物中酸性最强的是(填化学式);
(4)⑨与④两种元素的最高价氧化物的水化物碱性较强的是(填化学式);
(5)①的单质与②最高价氧化物的水化物浓溶液反应的化学方程式是;当消耗4.8g①的单质时,转移电子数为。
Ⅰ.①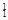 H与
H与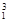 H;②O2与O3;③正丁烷(CH3CH2 CH2 CH3)与异丁烷
H;②O2与O3;③正丁烷(CH3CH2 CH2 CH3)与异丁烷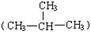 ;④甲烷(CH4)与丙烷(C3H8)。
;④甲烷(CH4)与丙烷(C3H8)。
(1)互为同位素的是______ (填序号,下同)。
(2)互为同系物的是______。
(3)互为同分异构体的是______。
(4)互为同素异形体的是______。
II.A~E等几种烃分子的球棍模型如下图所示,据此回答下列问题。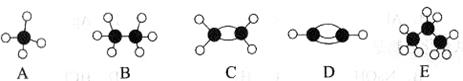
(1)D的电子式为___________,A的二氯取代物有种。
(2)可作为植物生长调节剂的是(填结构简式);
(3)A与氯气反应可以生成多种物质,试任写其中一个反应的化学方程式:;
(4)C与水在一定条件下反应的化学方程式为:。