(14分,每空2分) I.合成氨工业对国民经济和社会发展具有重要的意义。其原理为:
I.合成氨工业对国民经济和社会发展具有重要的意义。其原理为:
N2(g)+3H2 (g)
(g)  2NH3(g) △H=" -92.4" kJ/mol 据此回答以下问题:
2NH3(g) △H=" -92.4" kJ/mol 据此回答以下问题:
(1)为了提高氨气的产率,可以选择的方法是 _______(填序号,错选扣分)。
① 升高温度 ② 增大压强 ③ 使用催化剂 ④ 及时分离出NH3
(2)对在密闭容器中进行的可逆反应:N2(g)+3H2(g) 2NH3(g),下列哪种情况下,
2NH3(g),下列哪种情况下,
说明该反应已经达到化学平衡状态____________________________________。
①N2的正反应速率是NH3的逆反应速率的1/2
②在恒容条件下,混合气体的压强保持不变
③N2、H2、NH3的物质的量之比为1:3:2
④单位时间内每生成3mol H2的同时有2mol NH3生成
⑤3mol N-N键断裂,同时有6mol N-H键断裂
(3)一定条件下,NH3在固定体积的密闭容器中发生分解反应(△H>0)并达平衡后,仅改变下表中反应条件x,该平衡体系中随x递增y递减的是________________(选填序号)。
| 选项 |
a |
b |
c |
d |
| x |
温度 |
温度 |
加入H2的物质的量 |
加入NH3的物质的量 |
| y |
NH3的物质的量 |
平衡常数K |
NH3的转化率 |
生成物物质的量总和 |
II.(1)在酸性溶液中,碘酸钾(KIO3)和亚硫酸钠可发生如下反应:
2IO3-+5SO32-+2H+===I2+5SO42-+H2O
生成的碘可以用淀粉溶液检验,根据反应溶液出现蓝色所需的时间来衡量该反应的速率。
某同学设计实验如下表所示:
| |
0.01mol·L-1 KIO3酸性溶液(含淀粉)的体积/mL |
0.01mol·L-1 Na2SO3溶液的体积/mL |
H2O的体积 /mL |
实验 温度 /℃ |
溶液出现蓝色时所需时间/s |
| 实验1 |
5 |
V1 |
35 |
25 |
--------- |
| 实验2 |
5 |
5 |
40 |
25 |
---------- |
| 实验3 |
5 |
5 |
V2 |
0 |
----------- |
该实验的目的是_______________________________________________________________
________________________________________________;
表中V1=___________mL.
(2)可逆反应C(s)+H2O(g)  H2(g)+CO(g),△H>0达到平衡后,改变某一外界条件(不改变物质的量的条件下),反应速率
H2(g)+CO(g),△H>0达到平衡后,改变某一外界条件(不改变物质的量的条件下),反应速率 与时间t的关系如右图。
与时间t的关系如右图。
①图中t4到t6段时引起平衡移动的条件可能是  ;
;
②图中表示平衡混合物中CO的含量最高的一段时间是 。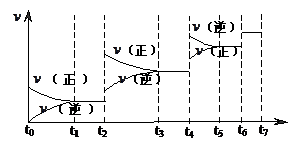
NO分子因污染空气而臭名昭著。近年来,发现少量的NO在生物体内许多组织中存在,它有扩张血管、免疫、增强记忆的功能,而成为当前生命科学的研究的热点。NO亦被称为“明星分子”。请回答下列问题。
(1)NO对环境的危害在于_________(填编号)。
| A.破坏臭氧层 | B.高温下能使一些金属被氧化 | C.造成酸雨 | D.与人体血红蛋白结合 |
(2)在含Cu+(亚铜离子)的酶的活化中心,亚硝酸根离子可转化为NO,写出Cu+和亚硝酸根离子在酸性水溶液中反应的离子方程式______________________________________
(3)在常温下,把NO气体压缩到100大气压,在一个体积固定的容器里加热到50℃,发现气体的压力迅速下降,压力降至略小于原压力2/3就不再改变,已知其中一种产物为N2O,写出上述变化的化学方程式_________________.
(4)解释变化(3)中为什么最后气体总压力小于原压力的2/3?__________________________.
(5)NO成为“臭名昭著的明星分子”所包含的哲学原理是_____________________________
为测定空气中CO2含量,做下述实验。
| 配0.1mol/L的标准盐酸和0.01mol/L的标准盐酸 |
→ |
用0.1mol/L的标准盐酸滴定未知Ba(OH)2溶液10mL用去盐酸19.60 mL |
→ |
用Ba(OH)2溶液吸收空气中的CO2 |
→ |
过 滤 |
→ |
取滤液20mL,用0.01mol/L的盐酸滴定用去盐酸34.8mL |
(1)为配置标准溶液,请选取必需的一组仪器。
①托盘天平②容量瓶③滴定管④量筒⑤烧杯⑥胶头滴管⑦玻璃棒
| A.①②⑤⑥ | B.②④⑤⑥⑦ | C.②①⑥⑦ | D.②④⑤⑥ |
(2)滴定操作时,左手,眼睛注视。
(3)取上述Ba(OH)2溶液10mL放入100mL容量瓶中,加水稀释至刻度,把稀释后的溶液放入密闭容器,并引入10L空气,振荡,过滤。需过滤的原因是。
(4)由实验数据算出空气中CO2的体积分数为。
(5)本实验中,若第一次滴定时使用的酸式滴定管未经处理,即更换溶液,进行第二次滴定,导致实验数据值(填偏高、偏低或无影响)。
剪长约6cm、宽2cm的铜片、铝片各一片,分别用接线柱平行地固定在一块塑料板上(间隔2cm)。将铜片与铝片分别和电流表的“+”、“-”端相连接,电流表指针调到中间位置。取两个50mL的小烧杯,在一个烧杯中注入约40mL的浓硝酸,在另一只烧杯中注入40mL0.5mol/L的硫酸溶液。试回答下列问题:
(1)两电极同时插入稀硫酸中,电流表指针偏向(填“铝”或“铜”)极,铝片上电极反应式为;
(2)两电极同时插入浓硝酸时,电流表指针偏向(填“铝”或“铜”)极,此时铝是(填“正”或“负”)极,铝片上电极反应式为。
2003年3月,中科院蒋锡夔院士和中科院上海有机化学所计国桢研究员因在有机分子簇集和自由基化学研究领域取得重大成果,而荣获国家自然科学一等奖。据悉,他们在研究过程中曾涉及到如下一种有机物。请根据所示化合物的结构简式回答问题:
(1)该化合物中,官能团⑦的名称是__________,官能团①的电子式是__________。该化合物是由______个氨基酸分子脱水形成的。写出该化合物水解生成的氨基酸的结构简式(任写一种)______________________________________________________,并写出此氨基酸与氢氧化钠溶液反应的化学方程式___________________________________________。
(2)上海有机化学研究所在我国氟化学理论研究和氟产品以及核化学工业等方面作出过重大贡献,如F46就是用的四氟乙烯与全氟丙烯共聚得到的,若两种单体物质的量之比1:1,试写出这种高聚物的结构简式______________________。已知三氟苯乙烯(三个氟均连在苯环上)的分子式为C8H5F3,则它的异构体除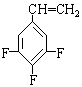 还有另外五种是_______________。
还有另外五种是_______________。
2002年诺贝尔化学奖的一半奖金授予了瑞士科学家库尔特维特里希,以表彰他“发明了利用核磁共振技术测定溶液中生物大分子三维结构的方法”。核磁共振技术是利用核磁共振谱来测定有机化合物结构,最有实用价值的就是氢谱,常用HNMR表示,如:乙醚分子中有两种氢原子,其HNMR谱中有两个共振峰,两个共振峰的面积比为3:2,而乙醇分子中有三种氢,HNMR谱中有三个峰,三个共振峰之间的面积比为3:2:1。
(1)请写出分子式C4H8在HNMR谱中两个峰面种为3:1的化合物的结构简式______。
(2)C4H10的HNMR谱有两种,其中作液体打火机燃料的C4H10的HNMR谱的两个峰的面积比为__________,结构简式__________;其同分异构体的两个峰的面种比为_________,结构简式为________________________。