我国第四套人民币硬币从1999年开始发行,一元币为钢芯镀镍(Ni),伍角币为钢芯镀铜合金,一角币为铝合金或不锈钢。
(1)铸造以上硬币用到的材料都是 (填“合成材料”或“金属材料”)。
(2)选择铸造硬币的材料不需要考虑的因素是 (填序号)。
| A.金属的导电性 | B.金属的耐腐蚀性 |
| C.金属的硬度 | D.金属价格与硬币面值的吻合度 |
(3)以上硬币涉及到Fe、Cu、Al、Ni(镍),已知Ni能够发生如下反应:
Ni+ H2SO4= NiSO4+ H2↑ Fe+ NiCl 2=" Ni" + FeCl 2
这两个反应的基本类型都是 。四种金属活动性由强到弱的顺序为 (用元素符号表示)。
取标准状况下2.24L某气态烃A置于密闭容器中,再通入足量的O2,用电火花引燃,燃烧产物的定量测定实验数据如下(图中的箭头表示气体的流向)。
试通过计算回答:
(1)烃A的分子式为 。
。
(2)写出烃A的所有同分异构体的结构简式:。
(3)某有机物B仅含碳、氢、氧三种元素,其相对分子质量大于100,小于106。已知A、B分子中所含的氢原子数相同,则B的分子式为。
已知A是来自石油的重要有机化工原料,E是具果香味的有机物,F是一种高聚物,可制成多种包装材料。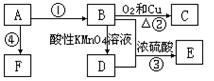
(1)A的最简式为:____________,C的名称:_____________,F的结构简式:____________________________________。
(2)D分子中的官能团名称是_________________,请设计一种实验来验证D物质存在该官能团的方法是_________________________________________。
(3)写出下列反应的化学方程式并指出反应类型:③____________________________,反应类型_____________。
已知乙烯能发生以下转化: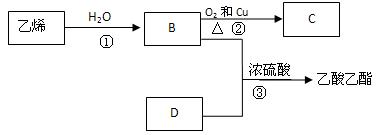
(1)乙烯的结构简式为:
(2)写出反应的化学方程式
①反应类型:
②反应类型:
③反应类型:
在101 kPa时,1.00 g C6H6(l)燃烧生成CO2和H2O(l)时,放出41.8 kJ的热量,表示C6H6燃烧热的热化学方程式为:__________________________________.
从海水中提取金属镁的生产步骤有:①浓缩结晶,②加熟石灰,③加盐酸,④过滤,⑤熔融电解,正确的生产步骤是。(填序号)