短周期元素A、B、C、D的原子序数依次递增,它们的原子序数之和为34,且原子最外层电子数之和为10;A、C原子的最外层电子数之和等于B原子的次外层电子数;A与C,B与D均为同主族元素。下列叙述正确的是
A. B、D的最高价氧化物都不能和酸反应
B.最高价氧化物对应的水化物的碱性:A>C
C.四种元素中B形成化合物的种类最多
D.A的原子半径为这四种当中最小的
下列说法不正确的是
| A.中秋佳节月饼中用小袋包装的生石灰来防止月饼氧化变质 |
| B.节能减排措施之一就是要发展低碳经济、循环经济,推广利用太阳能、风能 |
| C.“血液透析”利用了胶体的性质 |
| D.绿色化学的核心是利用化学原理从源头上减少和消除工业生产对环境的污染 |
已知:还原性HSO3¯>I¯,氧化性IO3¯> I2。在含3 mol NaHSO3的溶液中逐滴加入KIO3溶液。加入KIO3和析出I2的物质的量的关系曲线如右图所示。下列不正确的是()
| A.0~b :3HSO3-+ IO3-= 3SO42-+ I-+ 3H+ |
| B.a点时消耗NaHSO3的物质的量为1.2 mol |
| C.b~c间I2是还原产物 |
| D.当溶液中I¯与I2的物质的量之比为5∶2时,加入的KIO3为1.8mol |
已知A 、B、C、D之间的转化关系如右图所示。下列说法正确的是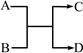
A.若A为Fe,D为氢气,则B一定为酸
B.若A、D为化合物,B为水,则C一定是气体单质
C.若A、B、C、D均为化合物,该反应一定属于复分解反应
D.若A、B、C、D均为10电子微粒,且C是可使湿润的红色石蕊试纸变蓝的气体,则D常温下一定呈液态
对以下实验装置图的说法正确的是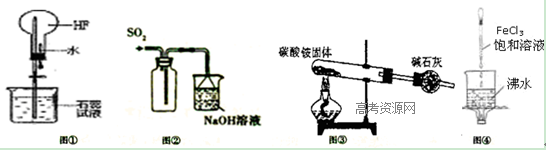
| A.利用图①装置做喷泉实验 |
| B.利用图②装置收集SO2并吸收尾气 |
| C.实验室里利用图③装置制取少量纯净的氨气 |
| D.利用图④装置制备氢氧化铁胶体 |
把500mLNH4HCO3和Na2CO3的混合溶液分成五等份,取一份加入含amol氢氧化钠的溶液恰好反应完全;另取一份加入含b mol HCl的盐酸恰好反应完全,则该混合溶液中c(Na+)为()
A.( )mol/L )mol/L |
B.(2b—a)mol/L | C.(l0b - 5a) mol/L | D.(5b一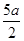 )mol/L )mol/L |