在一个容积固定不变的密闭容器中进行反应:2A(g)+B(g) 3C(g)+D(s),已知将2molA和1molB充入该容器中,反应在某温度下达到平衡时,C的物质的量为Wmol,C在平衡混合气体中的体积分数为n%。
3C(g)+D(s),已知将2molA和1molB充入该容器中,反应在某温度下达到平衡时,C的物质的量为Wmol,C在平衡混合气体中的体积分数为n%。
(1)可认定上述可逆反应在一定条件下已达到化学平衡状态的是 (选填序号)。
A. 体系压强不再变化 B. v正(A)=2v逆(B)
C. 体系的密度不再变化 D. 混合气体的平均相对分子质量不再变化
(2)如果用下列情况的配比作起始物,在同样的容器和温度下达到平衡,其结果一定是:
C的物质的量为2Wmol,C在平衡混合气体中的体积分数仍为n%的是
A. 4molA+2molB B. 6molC+1molD
C. 1molA+0.5molB+1.5molC+0.5molD D. 2molA+1molB+3molC+1molD
E. 2molA+1molB+3molC+2molD (4)若维持该题条件不变,
(4)若维持该题条件不变, 仅从生成物开始配比,要求达到平衡时,C的物质的量仍为Wmol,则D的起始物质的量n(D)应满足的条件是 (用含W的代数式表示
仅从生成物开始配比,要求达到平衡时,C的物质的量仍为Wmol,则D的起始物质的量n(D)应满足的条件是 (用含W的代数式表示 )
)
(5)此反应的v—t图象如甲图,若其他条件都不变,只是在反应前加入合适的催化剂,则
其v—t图象如乙图,请用“=、<、>”填空: a1 a2;两图中阴影部分面积:甲 乙。
现有稀盐酸、稀硫酸、氢氧化钡、碳酸钠四瓶失去标签的溶液,分别编号为A、B、C、D每次取少量溶液两两混合,所观察到的现象如表,“一”表示无明显现象;“↓”表示有沉淀生成;“↑”表示有气体生成。
(1)则A,B,
C,D;(写化学式)
(2 )写出实验过程中有关物质间反应的离子方程式
)写出实验过程中有关物质间反应的离子方程式
B +C
如图所示,在一烧杯中盛有H2SO4溶液,同时有一表面光滑的塑料小球悬浮于溶液中央,向该烧杯中缓缓注入 Ba(OH)2溶液至恰好完全反应[设H2SO4和Ba(OH)2溶液密度相同]。试回答:
(1)此实验中,观察到的现象有
① ,
,
②。
(2)写出实验过程中反应的离子方程式。
现有mg某气体,它由双原子分子构成,它的摩尔质量为Mg·mol-1。若阿伏加德罗常数用NA表示,则:
(1)该气体所含原子总数为个;
(2)该气体在标准状况下的体积为____________L;
(3)该气体每个分子的质量为g;
(4)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为mol/L。
将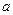 g金属钠投入到
g金属钠投入到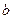 g水(足量)中。
g水(足量)中。
(1)所得溶液中溶质的质量分数为 ;
(2)能否求溶液中溶质的物质的量浓度?为什么? ;
;
(3)所得溶液中Na+与H2O的个数比为 。
化工生产中常常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱 ”指烧碱和纯碱。
”指烧碱和纯碱。
(1)从物质的分类角度看,不恰当的一种物质是___________ 。
(2)“三酸”与“两碱”之间均可反应,若用化学方程式表示有六个(酸过量时),若用离子方程式表示却只有两个,请写出这两个离子方程式(酸过量时)。
__________________________________;
。