某二元酸(化学式H2A)在水中的电离方程式是:H2A = H+ + HA-,HA- H++A2-,又知0.1mol·L-1NaHA溶液的pH = 2。则下列说法不正确的是
H++A2-,又知0.1mol·L-1NaHA溶液的pH = 2。则下列说法不正确的是
A.因为A2-+H2O  HA-+OH-,所以Na2A溶液显碱性
HA-+OH-,所以Na2A溶液显碱性
B.0.1mol·L-1 H2A溶液中氢离子的物质的量浓度为0.11 mol·L-1
C.NaHA溶液中各种离子浓度的关系是c(Na+ ) > c(HA-) > c(H+) > c(A2-) > c(OH-)
D.在NaHA溶液中,HA-电离的趋势大于其水解的趋势
某同学组装了如图所示的电化学装置,则下列说法正确的是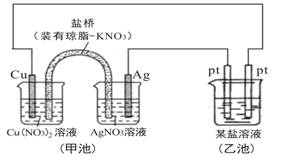
| A.图中甲池为原电池装置,Cu电极发生还原反应 |
| B.实验过程中,甲池左侧烧杯中NO3-的浓度不变 |
| C.若甲池中Ag电极质量增加5.4g时,乙池某电极析出1.6g金属,则乙中的某盐溶液可能是AgNO3溶液 |
| D.若用铜制U形物代替“盐桥”,工作一段时间后取出U形物称量,质量会减小 |
下列说法不正确的是
A.激素类药物乙烯雌酚的结构简式为: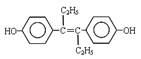 ,它的分子式是:C18H20O2 ,它的分子式是:C18H20O2 |
| B.等质量的甲烷、乙烯、乙醇分别充分燃烧,所耗用氧气的量依次减少 |
C.聚乳酸(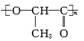 )是由单体之间通过加聚反应合成的 )是由单体之间通过加聚反应合成的 |
D.实验证实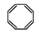 可使溴的四氯化碳溶液褪色,说明该分子中存在碳碳双键 可使溴的四氯化碳溶液褪色,说明该分子中存在碳碳双键 |
a-5X、b-3Y、aZ、bW、a+4T均为短周期元素,其原子半径随原子序数变化如下图所示。Z是地壳中含量最高的金属元素,W原子最外层电子数是K层电子数的2倍。则下列说法正确的是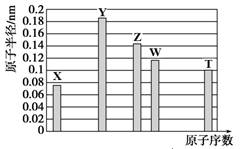
| A.Z、T两种元素的离子半径相比,前者较大 |
| B.X、Y形成的两种化合物中,阴、阳离子物质的量之比分别为1∶1和1∶2 |
| C.X、W、T三种元素的气态氢化物中,稳定性最差的是W的氢化物,沸点最高的是T的氢化物 |
| D.Y、T两种元素的最高价氧化物对应的水化物均能溶解X和Z形成的常见化合物 |
下列说法正确的是
| A.实验中要配制500 mL 0.2 mol·L-1 KCl溶液,需用托盘天平称量7.45g KCl固体 |
| B.实验室制氢气,为了加快反应速率,可向稀H2SO4中滴加少量Cu(NO3)2溶液 |
| C.排除碱式滴定管尖嘴端气泡时,可以向上弯曲橡皮管,然后挤压玻璃球,排出气泡 |
| D.往含有FeBr2和FeI2的混合溶液中通入足量的氯气,然后把溶液蒸干、灼烧,得到FeCl3固体 |
下列说法不正确的是
| A.发展核电、煤中加入生石灰、利用二氧化碳制造全降解塑料都能有效减少环境污染 |
| B.物质变化中炭化、钝化、皂化、酯化、熔化都属于化学变化 |
| C.氢键、分子间作用力、离子键和共价键均为微粒间的相互作用力 |
| D.农业废弃物、城市工业有机废弃物及动物粪便中都蕴藏着丰富的生物质能 |