下列关于Cl2的描述中,正确的是
| A.液氯可以密封保存在钢瓶中 |
| B.红热的铜丝在Cl2中燃烧后生成蓝色的CuCl2 |
| C.过量的铁在Cl2中燃烧生成氯化亚铁 |
| D.Cl2以液态形式存在时可称作氯水或液氯 |
某强酸的pH=" a" ,强碱的pH=" b" 。已知a + b = 12,若酸碱溶液混合后pH= 7,则酸溶液体积V1与碱溶液体积V2的正确关系
| A.V1=102V2 | B.V2=102V1 | C.V1=2V2 | D.V2=2V1 |
1体积pH=2.5的盐酸与10体积某一元强碱溶液恰好完全反应,则该碱溶液的pH
| A.9.0 | B.9.5 | C.10.5 | D.11.5 |
应2X(g)+Y(g) 2Z(g);△H<0(正反应为放热反应)。在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量[n(Z)]与反应时间(t)的关系如图所示。则下列判断正确的是
2Z(g);△H<0(正反应为放热反应)。在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量[n(Z)]与反应时间(t)的关系如图所示。则下列判断正确的是
| A.T1<T2,P1<P2 | B.T1<T2,P1>P2 | C.T1>T2,P1>P2 | D.T1>T2,P1<P2 |
在一定温度下,反应1/2H2(g)+ 1/2X2(g) 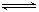 HX(g)的平衡常数为10。若将1.0mol的HX(g)通入体积为1.0L的密闭容器中,在该温度时HX(g)的最大分解率接近于
HX(g)的平衡常数为10。若将1.0mol的HX(g)通入体积为1.0L的密闭容器中,在该温度时HX(g)的最大分解率接近于
| A.5% | B.17% | C.25% | D.33% |
一定温度下,l mol X和n mol Y在体积为2L的密闭容器中发生如下反应:X(g)+Y(g) 2Z(g)+M(s),5min后达到平衡,此时生成2a mol Z。下列说法正确的是
2Z(g)+M(s),5min后达到平衡,此时生成2a mol Z。下列说法正确的是
| A.用X表示此反应的反应速率是(0.1—0.2a)mol·(L·min)-1 |
| B.当混合气体的质量不再发生变化时,说明反应达到平衡状态 |
| C.向平衡后的体系中加入l mol M,平衡向逆反应方向移动 |
| D.向上述平衡体系中再充入l mol X,v(正)增大,v(逆)减小,平衡正向移动 |