卤代烃的取代反应,实质是带负电荷的原子团取代了卤代烃中的卤原子,例如:CH3Br+OH-(或NaOH)→CH3OH+Br-(或NaBr)。下列反应的化学方程式中,不正确的是
| A.CH3CH2Br+NaHS→CH3CH2SH+NaBr |
| B.CH3I+CH3ONa→CH3O CH3+NaI |
| C.CH3CH2Cl+CH3ONa→CH3Cl+CH3CH2ONa |
| D.CH3CH2Cl+CH3CH2 ONa→(CH3CH2)2O+NaCl |
发展混合动力车是实施节能减排的重要措施之一。汽车上坡或加速时,电动机提供推动力,降低了汽油的消耗;在刹车和下坡时电动机处于充电状态以节省能耗。混合动力车的电动机目前一般使用的是镍氢电池,镍氢电池采用镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)电解液。镍氢电池充放电原理如右图,其总反应式为:H2+2NiOOH 2Ni(OH)2。下列有关混合动力车的判断正确的是
2Ni(OH)2。下列有关混合动力车的判断正确的是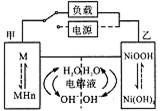
| A.在上坡或加速时,乙电极周围溶液的pH将减小 |
| B.在上坡或加速时,溶液中的K+向甲电极迁移 |
C.在刹车和下坡时,甲电极的电极反应式为:2 H2O+2e- |
| D.在刹车和下坡时,乙电极增重 |
短周期元素X、Y、Z,其中X、Y位于同一主族,Y、Z位于同一周期。X原子的最外层电子数是其电子层数的3倍,Z原子的核外电子数比Y原子少1。下列比较正确的是
| A.元素非金属性:Z> Y > X | B.最高价氧化物水化物酸性:Z > Y |
| C.原子半径:Z < Y < X | D.气态氢化物的稳定性:Z < Y < X |
下列离子方程式中正确的是
| A.向Ba(OH)2溶液中滴加NaHSO4溶液至恰好为中性: Ba2+ + OH- + H+ + SO42-= BaSO4↓+ H2O |
B.NH4HCO3溶液与过量KOH浓溶液共热:NH4++ OH-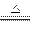 NH3↑+ H2O NH3↑+ H2O |
| C.稀硝酸和过量的铁屑反应:3 Fe + 8H+ +2 NO3- =" 3" Fe3+ +2 NO↑ + 4 H2O |
| D.KI溶液与H2SO4酸化的H2O2溶液混合:2 I- + H2O2 + 2 H+ ="2" H2O + I2 |
已知辛烷的燃烧热为5518kJ·mol-1,强酸与强碱在稀溶液中发生反应时的中和热为
57.3kJ·mol-1,则下列热化学方程式书写正确的是
①C8H18(l)+25/2O2(g)8CO2(g)+9H2O(g);△H=-5518kJ·mol-1
②2C8H18(l)+25O2(g)16CO2(g)+18H2O(l);△H=-11036kJ·mol-1
③H+(aq) + OH-(aq) H2O(l); △H="" +57.3kJ·mol-1
④2NaOH(aq) +H2SO4(aq) Na2SO4(aq) + 2H2O(l);△H=-57.3kJ·mol-1
| A.①③ | B.②③ | C.②④ | D.只有② |
下列推断正确的是
| A.SiO2 是酸性氧化物,能与NaOH溶液反应 |
| B.Na2 O、Na2 O2组成元素相同,与 CO2反应产物也相同 |
| C.CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 |
| D.新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色 |