(8分) 选择下列实验方法分离物质,将分离方法的序号填在横线上。
A.萃取 分液法 分液法 |
B.加热分解法 | C.结晶法 | D.分液法 E.蒸馏法 F.过滤法 |
(1)________从KNO3和NaCl的混合溶液中获得KNO3。
(2)________分离水和汽油的混合物。
(3)________分离四氯化碳(沸点76.75℃)和甲苯(沸点110.6℃)的混合物。
(4)________从NaCl与NH4HCO3固体混合物中得到NaCl。
(1)向Na2CO3的浓溶液中逐滴加入稀盐酸,直到不再生成CO2气体为止,则在此过程中,溶液的c(HCO3- )变化趋势可能是:①逐渐减小;②逐渐增大;③先逐渐增大,而后减小;④先逐渐减小,而后增大。4种趋势中可能的是 。
(2)pH相同的HCl溶液、H2SO4溶液、CH3COOH溶液各100 mL。
①3种溶液中,物质的量浓度最大的是 。
②分别用pH为0.1的NaOH溶液中和,其中消耗NaOH溶液最多的是 。
③反应开始时,反应速率 。
| A.HCl最快 | B.H2SO4最快 | C.CH3COOH最快 | D.一样快 |
某学生用0.2000mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
①用蒸馏水洗涤碱式滴定管,注入0.2000mol·L-1的标准NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体;
③调节液面至“0”或“0”刻度线稍下,并记下读数;
④量取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液;
⑤用标准液滴定至终点,记下滴定管液面读数。
⑥重复以上滴定操作2-3次。
请回答:
(1)以上步骤有错误的是(填编号)________,该错误操作会导致测定结果_________
(填“偏大”、“偏小”或“无影响”)。
(2)步骤④中,量取20.00mL待测液应使用__________________(填仪器名称),在锥形瓶装液前,留有少量蒸馏水,测定结果____________(填“大”、“偏小”或“无影响”)。
(3)步骤⑤滴定时眼睛应注视 _______________________________判断到达滴定终点的依据是:__________________________________________________。
(4)以下是实验数据记录表
| 滴定次数 |
盐酸体积(mL) |
NaOH溶液体积读数(mL) |
|
| 滴定前 |
滴定后 |
||
| 1 |
20.00 |
0.00 |
18.10 |
| 2 |
20.00 |
0.00 |
16.30 |
| 3 |
20.00 |
0.00 |
16.22 |
从上表可以看出,第1次滴定记录的NaOH溶液体积明显多于后两次的体积,其可能的原因是()
A.滴定前滴定管尖嘴有气泡,滴定结束无气泡
B.锥形瓶用待测液润洗
C.NaOH标准液保存时间过长,有部分变质
D.滴定结束时,俯视计数
(5) 根据上表记录数据,通过计算可得,该盐酸浓度为:____________mol·L-1
乙二酸俗名草酸,某化学学习小组的同学欲探究测定草酸晶体(H2C2O4·xH2O)中x值。通过查阅资料该小组同学通过网络查询得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:
2MnO4-+5H2C2O4+6H+2Mn2++10CO2↑+8H2O
该组同学设计了滴定的方法测定x值。
①称取1.260 g纯草酸晶体,将其酸制成100.00 mL水溶液为待测液。
②取25.00 mL待测液放入锥形瓶中,再加入适量的稀H2SO4
③用浓度为0.1000 mol/L的KMnO4标准溶液进行滴定,达到终点时消耗10.00 mL;
请回答:
⑴滴定时,将KMnO4标准液装在下图中的(填“甲”或“乙”)滴定管中。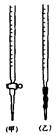
⑵本实验滴定达到终点的标志是
⑶通过上述数据,计算出x=。
讨论:①若滴定终点时俯视滴定管刻度,则由此测得的x值会(填“偏大”、“偏小”或“不变”,下同)。
②若滴定时所用的KMnO4溶液因久置而导致浓度变小,则由此测得的x值会
为比较Fe3+和Cu2+对H2O2分解的催化效果甲乙两组同学分别设计了如图一、图二所示的实验。
(1)图一可通过观察_____________________________ 现象来定性比较得出结论。有同学提出将CuSO4改为CuCl2更为合理,其理由是__________________________,
你认为还可以作其他 何种改进? _____________________________________________。
何种改进? _____________________________________________。
(2)图二可用于定量比较反应的快慢,检查图二装置气密性的方法是。
利用图二做实验时需测量的数据是。
(12分) 在浓CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙(粒子直径在1~100nm之间)。下图所示A~E为实验室常见的仪器装置(部分固定夹持装置略去),请根据要求回答问题。
在浓CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙(粒子直径在1~100nm之间)。下图所示A~E为实验室常见的仪器装置(部分固定夹持装置略去),请根据要求回答问题。
(1)写出实验室制取NH3的化学方程式。
(2)实验室制取、收集干燥的NH3 ,需选用上述仪器装置的接口连接顺序是(选填字母):a接,接,接h;
,需选用上述仪器装置的接口连接顺序是(选填字母):a接,接,接h;
(3)用如图所示装置也可以制取NH3,则圆底烧瓶中的固体可以选用(选填字母编号);
| A.碱石灰 | B.生石灰 | C.无水氯化钙 | D.无水硫酸铜 E.烧碱 |
(4)向浓CaCl2溶液中通人NH3和C02气体制纳米级碳酸钙时,应先通人的气体是,试写出制纳米级碳酸钙的化学方程式;
(5)试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级