某学生用0.2000mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步:
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④移取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数。 请回答:
(1)以上步骤有错误的是(填编号)_____,该错误操作会导致测定结果
(填“偏大”、“偏小”或“无影响”)__________________
(2)步骤⑤中,在记下滴定管液面读数时,滴定管尖嘴有气泡,将导致测定结果(填“偏大”、“偏小”或“无影响”)___________________
(3)判断滴定终点的现象是:锥形瓶中溶液从 色变为 色,且半分钟不变色。
(4)下图是某次滴定时的滴定管中的液面,其读数为 mL
(5)根据下列数据:请计算待测盐酸溶液的浓度: mol/L
| 滴定次数 |
待测液体积(mL) |
标准烧碱体积(mL) |
|
| 滴定前读数(mL) |
滴定后读数(mL) |
||
| 第一次 |
20.00 |
0.40 |
20.40 |
| 第二次 |
20.00 |
4.00 |
24.00 |
| 第三次 |
20.00 |
2.00 |
24.10 |
用18 mol·L-1浓硫酸配制100 mL 3.0 mol·L-1稀硫酸的实验步骤如下:
①计算所用浓硫酸的体积 ②量取一定体积的浓硫酸 ③溶解 ④ ⑤转移、洗涤 ⑥定容、摇匀 ⑦装瓶贴标签
完成下列问题:
(1)所需浓硫酸的体积是 ,量取浓硫酸所用的量筒的规格是 (从下列中选用A.10 mL B.25 mL C.50 mL D.100 mL)。
(2)第③步实验的操作是 。
(3)下列情况对所配制的稀硫酸浓度有何影响?(用“偏大”“偏小”“无影响”填写)
A.所用的浓硫酸长时间放置在密封不好的容器中_______________________;
B.容量瓶用蒸馏水洗涤后残留有少量的水________________;
C.所用过的烧杯、玻璃棒未洗涤________________;
D.定容时俯视刻度线________________。
已知硫酸铜在加热条件下发生分解反应,生成氧化铜、二氧化硫、三氧化硫和氧气。请用右图所示装置,测定硫酸铜在加热分解时产生的各物质与参加反应的硫酸铜的物质的量的关系。实验测得数据和有关结果如下: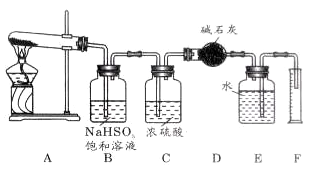
①准确称得无水硫酸铜 2.4 g;
②测出量筒中水的体积,折算成标准状态下气体的体积为112 mL;
③干燥管在实验后质量增加1.28 g;
④实验结束时装置B中的NaHSO3溶液变为Na2SO4溶液(不含其他溶质)。
请回答下列问题:
(1)装置B的作用是_________________ ;发生的化学方程式___________________。
(2)装置C的作用是_______________________;干燥管收集到的物质是__________ 。
(3)装置E和F的作用是________________________________;
(4)实验数据测出后,首先应计算出的物质是_________,有________mol;并据此计算出SO2为_________mol,SO3为___________mol。
用MnO2和浓盐酸制取纯净干燥的氯气,并让氯气与铜粉反应制取纯净的无水CuCl2,装置如下图所示。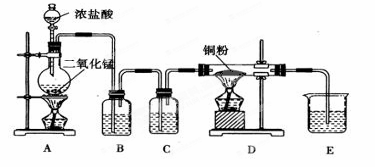
回答下列问题:
(1)B中选用的试剂是饱和食盐水,其作用是__________;C中选用的试剂是__________,其作用是_________
(2)D中反应的化学方程式是_____________,将此生成物溶于少量水,得到______________色溶液。
(3)某学生应用如图所示的方法研究物质的性质,其中气体X的主要成分是氯气,杂质是空气和水蒸气。回答下列问题:
①该项研究(实验)的主要目的是____________________________。
②与研究目的直接相关的实验现象是________________________。
③从物质性质的方面来看,这样的实验设计还存在事故隐患,事故表现是____________。
④请在图中的D处以图的形式表明克服事故隐患的措施。
海洋植物如海带中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室从海带中提取碘的流程图如下:(已知:Cl2+2I-==2Cl-+I2)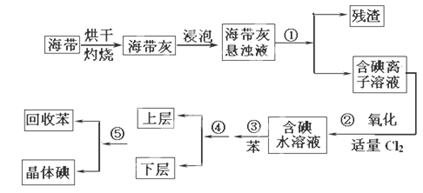
(1)指出提碘的过程中有关的实验操作名称:① ,③ ,④ 。
(2)操作③、④可以分解为如下几步:
A、旋开活塞,用烧杯盛接溶液
B、从分液漏斗上口倒出上层溶液
C、打开分液漏斗上口玻璃塞或使塞上的凹槽对准漏斗上口的小孔
D、静置,分层
E、把盛有溶液的分液漏斗放在铁架台的铁圈上
F、把50mL碘水和15mL苯加入分液漏斗中,盖好玻璃塞
G、检查分液漏斗是否漏液
H、倒转分液漏斗,振荡
(i)正确的操作顺序是:G→ → E → D → → →B。
(ii)能选用苯做萃取剂的原因是: 。
(iii)上述(C)这样操作的目的是: 。
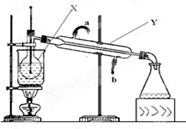
(3)从流程图中,将操作④后的 层液体(填 “上”或“下”)用右图仪器进行操作⑤,写出仪器的名称:X Y 。请指出右图装置中存在的一处错误: 。
(10分)某小组以CoCl2•6H2O、NH4Cl、H2O2、浓氨水为原料,在活性炭催化下,合成了橙黄色晶体X.为确定其组成,进行如下实验。
①氨的测定:精确称取w g X,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,用V1 mL cl mol•L﹣1的盐酸标准溶液吸收.蒸氨结束后取下接收瓶,用c2 mol•L﹣1NaOH标准溶液滴定过剩的HCl,到终点时消耗V2 mL NaOH溶液.
氨的测定装置(已省略加热和夹持装置)
②氯的测定:准确称取样品X,配成溶液后用AgNO3标准溶液滴定,K2CrO4溶液为指示剂,至出现淡红色沉淀不再消失为终点(Ag2CrO4为砖红色)。
回答下列问题:
(1)装置中安全管的作用原理是________________。
(2)用NaOH标准溶液滴定过剩的HCl时,应使用_____________式滴定管,可使用的指示剂为____________。
(3)样品中氨的质量分数表达式为_____________。
(4)测定氨前应该对装置进行气密性检验,若气密性不好测定结果将__________(填“偏高”或“偏低”)。
(5)测定氯过程中,使用棕色滴定管的原因是_________;滴定终点时,若溶液中c(Ag+)=2.0×10-5 mol•L﹣1,c(CrO42-)为__________mol•L-1。已知:Ksp(Ag2CrO4)=1.12×10-12
(6)经测定,样品X中钴、氨和氯的物质的量之比为1:6:3,钴的化合价__________,制备X的化学方程式为__________;X的制备过程中温度不能过高的原因是__________。