高效净水剂聚合氯化铝铁(PAFC)的组成可表示为[AlFe(OH)nCl6-n]m,该物质广泛应用于
日常生活用水 和工业废水的处理。
和工业废水的处理。
(1)为检测PAFC中Al和Fe含量,采用如图所示流程进行。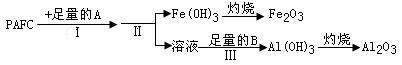
回答下 列问题:
列问题:
①PAFC中铁元素的化合价为_________。
②步骤I中的试剂A是______ ___(填“氨水”或“氢氧化钠溶液”)。
③步骤Ⅱ的名称是 。
④步骤Ⅲ的离子方程式为_________________________________ __。
(2)某工厂欲以工业废料(金属铝、铁及其氧化物)为原料制取PAFC,设计如下流程:
①所得酸性溶液中,不能确定是否一定存在的阳离子是___________
A、Al3+ B、Fe2+ C、Fe3+ D、H+
为证明该离子确实存在,可采用的试剂是_____________________。
②往酸性 溶液中加入试剂X的目的是_________________________________。
溶液中加入试剂X的目的是_________________________________。
工业上利用硫酸渣(含Fe2+、Fe3+的硫酸盐及少量CaO和MgO)制备高档颜料铁红(Fe2O3 )和回收(NH4)2SO4,具体生产流程如下:
|

(1)在废渣溶解操作时,应选用__________溶解(填字母)。
| A.氨水 | B.氢氧化钠 | C.盐酸 | D.硫酸 |
(2)物质A是一种氧化剂,工业上最好选用(供选择使用的有:空气、Cl2、MnO2),其理由是 。
(3)根据下图有关数据,你认为工业上氧化操作时应控制的条件是:
。
(4)“结晶”反应的化学方程式为
。
(5)简述检验“滤液”中含有NH4+的实验方法:
。
A、D、E、X、Y是原子序数依次增大的短周期主族元素。其中X原子最外层电子数是内层电子总数的3倍;X、Y同族;A与X、Y既不同族也不同周期;D元素的某种同位素原子在考古方面有重要应用。
(1)Y的离子结构示意图为。
(2)钠、A和X三种元素组成的化合物,其所含的化学键类型有。
(3)甲由A、E两种元素组成,分子中含有18个电子,只存在共价单键。常温下甲是一种无色液体。
①甲是一种二元弱碱,写出其 一级电离方程式:。
一级电离方程式:。
②甲在碱性溶液中能够将CuO还原为Cu2O,已知每1mol甲参加反应有 4 mol电子转移,该反应的化学方程式为:。
(4)处理含DX、YX2烟道气污染的一种方法,是在催化剂作用下使两者反应,产物之一为单质Y。已知反应生成1 g Y固体单质时放出8.4 k J热量,此反应的热化学方程式为。
J热量,此反应的热化学方程式为。
(5)将0.050 mol YX2(g)和0.030 mol X2(g)放入容积为1 L的密闭容器中,反应:
X2(g) +2YX 2(g) 2YX3(g)在一定条件下达到平衡。
2YX3(g)在一定条件下达到平衡。
①若其他条件不变,增大体系的压强,平衡常数K(填“增大”、“减小”或“不变”)。
②平衡时测得c(X2)=0.010 mol·Lˉ1。该条件下反应的平衡常数K=,YX2的平衡转化率为。
碳和碳的化合物在人类生产、生活中的应用非常广泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是一种理想,更是一种值得期待的新的生活方式。
(1)甲烷燃烧放出大量的热,可作为能源用于人类的生产和生活。
已知:①2CH4(g)+3O2(g)=2CO(g)+4H2O(l);△H1= —1214kJ/mol
②2CO(g)+O2(g)=2CO2(g);△H2= —566kJ/mol
则反应CH4(g)+2O2(g)=CO2(g)+2H2O(l)的△H=。
(2)①将两个石墨电极插入KOH溶液中,向两极分别通入CH4和O2,构成甲烷燃料电池。其正极电极反应式是:。
②某同学利用甲烷燃料电池设计了一种电解法制取Fe(OH)2的实验装置(如下图所示),通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法中正确的是(填序号)
A.电源中的a一定为正极,b一定为负极
B.可以用NaCl溶液作为电解液
C.A、B两端都必须用铁作电极
D.阴极发生的反应是:2H+ + 2e-→H2↑
③若将 所得Fe(OH)2沉淀暴露在空气中,反应的化学方程式为。
所得Fe(OH)2沉淀暴露在空气中,反应的化学方程式为。
(3)将不同量的CO(g)和H2O(g)分别通入体积为2L的恒容密闭容器中,进行反应:
CO(g)+H2O(g) CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
| 实验组 |
温度/℃ |
起始量/mol |
平衡量/mol |
达到平衡所需时间/min |
|
| H2O |
CO |
CO2 |
|||
| 1 |
650 |
2 |
4 |
1.6 |
5 |
| 2 |
900 |
1 |
2 |
0.4 |
3 |
| 3 |
900 |
a |
b |
c |
1 |
①实验1中,以v(H2)表示的平均反应速率为。
②该反应的正反应为(填“吸”或“放”)热反应。
(4)将2.4g碳(碳的相对原子质量为12)在足量氧气中燃烧,所得气体通入100mL 3.0mol/L的氢氧化钠溶液中,完全吸收后,溶液中的溶质的化学式是;溶液中所含离子的物质的量浓度由大到小的顺序为:。
化合物B是生活中一种常见的有机物,制取E和F的转化关系如下图所示。已知C能使溴水褪色,F有果香味。
(1)指出反应类型:①;③。
(2)C的分子式为:。
(3)写出②转化的化学方程式:②。
(4)F有多种同分异构体,写出其中两种的结构简式、。
现有部分前四周期元素的性质或原子结构如下表:
| 元素编号 |
元素性质或原子结构 |
| A |
原子的电子排布图为 |
| B |
常温下单质为双原子分子,原子间形成三对共用电子对 |
| C |
原子的s轨道电子数等于p轨道电子数,元素的最低负价为-2价 |
| D |
二价阳离子与C的阴离子具有相同的电子层结构 |
| E |
原子序数是D两倍, |
根据以上情况,回答下列问题:(答题时A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为;
(2)B的氢化物的分子空间构型是,该氢化物的等电子体是;
(3)E的价电子排布式是,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2∶1,三个氯离子位于外界,ECl3形成的配合物的化学式为;
(4)AC2在高温高压下所形成的晶胞如右图所示。该晶体的类型属于(选填“分子”、“原子”、“离子”或“金属”)晶体,该晶体中A原子的杂化形式为;
(5)D 的单质在空气中燃烧发出耀眼的白光,请用原子结构
的知识解释发光的原因:。