利用过滤的方法可以初步除去粗盐中的泥沙等不溶性的杂质,但仍含有CaCl2,CaCl2是一种易溶于水的物质,无法用过滤的方式将其和NaCl分离,经过分析讨论,某小组同学在此基础上继续设计了如下实验:
回答下列问题:
(1)该小组同学的实验目的是 ;
(2)上图括号内的操作步骤 为① ② ;
为① ② ;
(3)按此实验方案得到的NaCl固体中肯定含有 (填化学式)杂质,为了解决这个问题可以向过滤得到的滤液中加入适量的 (填名称)。
(4)写出上述实验中加入过量Na2CO3后发生反应的化学方程式 。
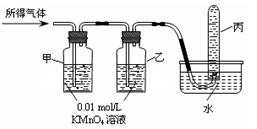
纯铁在冷的浓硫酸中能发生钝化。某兴趣小组同学发现将一定量的纯铁与浓硫酸加热时,铁完全溶解,得到溶液A,并产生大量气体B。实验室现有下列试剂:0 .01 mol/L 酸性KMnO4溶液、0.1 mol/L KI溶液、3%H2O2溶液、淀粉溶液、蒸馏水。请你协助他们探究所得溶液和气体的成分,并将有关实验操作、预期现象和结论填入下列表格中。
.01 mol/L 酸性KMnO4溶液、0.1 mol/L KI溶液、3%H2O2溶液、淀粉溶液、蒸馏水。请你协助他们探究所得溶液和气体的成分,并将有关实验操作、预期现象和结论填入下列表格中。
[提出猜想]
Ⅰ.所得溶液中的金属离子可能含有Fe2+和Fe3+中的一种或两种;
Ⅱ.所得气体中可能含有中的一种或两种。
Ⅲ.任意写出一个铁与浓硫酸加热时,可能发生的有关反应方程式
[实验探究]
实验操作 |
预期现象 |
结论 |
|
| 验证猜想Ⅰ |
步骤①:取少量溶液A,滴入0.01 mol/L 酸性KMnO4溶液 |
||
| 步骤②: |
含有Fe3+ |
||
| 验证猜想Ⅱ |
将所得气体B通入如下图装置 |
含有两种气体 |
[问题讨论]
有同学提出,若另外选用KSCN溶液,则
仅利用KSCN和H2O2两种溶液即可完成
猜想Ⅰ的所有探究,请对该观点进行评价:
。
某化学课外活动小组研究乙醇氧化的实验并验证其产物,设计了甲、乙两套装置(图中的夹持仪器均未画出,"△"表示酒精灯热源),每套装置又可划分为①、②  、③三部分。仪器中盛放的试剂为:a-无水乙醇(沸点:78 ℃);b
、③三部分。仪器中盛放的试剂为:a-无水乙醇(沸点:78 ℃);b  -铜丝;c-无水硫酸铜;d-新制氢氧化铜悬浊液。
-铜丝;c-无水硫酸铜;d-新制氢氧化铜悬浊液。 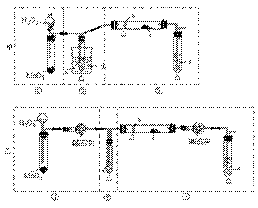
(1)对比两套方案,简述各自的优点:
甲_______________________________
________________________________。
乙_______________________________
________________________________。
(2)集中两套方案的优点,组成一套比较合理完善的实验装置,可按气流由左至右的顺序表示为1.甲①(接干燥管) 2. _______ 3. _______(例如甲①,乙②)
(3)实验中钢丝的作用是_________________。
(4)实验中能验证乙醇氧化产物的实验现象是______________________________________。
(5)装置中,若撤去第①部分,其它操作不变,则无水硫酸铜无明显变化,其余现象与(4)相同,推断燃烧管中主要反应的化学方程式_________________________。
某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用下图所示装置进行有关实验。请回答:
(1) 装置A中发生的化学反应方程式为。(2) 装置D中试管口放置的棉花中应浸一种液体,这种液体是  ,
,
其作用是 。
(3) 装置B的作用是贮存多余的气体。当D处有明显的现象后,关闭旋塞K并移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中现象是。_B中应放置的液体是(填字母) 。
a.水 b.酸性KMnO4溶液 c.浓溴水 d.饱和NaHSO3溶液
(4) 实验中,取一定质量的铜片和一定体积18 mol·L—1的浓硫酸放在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
① 有一定量的余酸但未能使铜片完全溶解,你认为原因是
。
② 下列药品中能用来证明反应结束后的烧瓶中确有余酸的是________(填字母)。
a.铁粉 b.BaCl2溶液 c.银粉 d.NaHCO3溶液
(9分)实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:4NH+6HCHO===3H++6H2O+(CH2)6N4H+[滴定时,1 mol(CH2)6N4H+与1 mol H+相当],然后用NaOH标准溶液滴定反应生成的酸.某兴趣小组用甲醛法进行了如下实验:
步骤Ⅰ 称取样品1.500 g.
步骤Ⅱ 将样品溶解后,完全转移到250 mL容量瓶中,定容,充分摇匀。
步骤Ⅲ 移取25.00 mL样品溶液于250 mL锥形瓶中,加入10 mL 20%的中性甲醛溶液,摇匀、静置5 min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点。按上述操作方法再重复2次。
(1)根据步骤Ⅲ填空:
①若碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数________(填“偏高”、“偏低”或“无影响”)。
②若锥形瓶用蒸馏水洗涤后,水未倒尽,则测得样品中氮的质量分数________(填“偏高”、“偏低”或“无影响”)。
③若滴定前,碱式滴定管尖嘴处有气泡,而在滴定后气泡消失,则测得样品中氮的质量分数________ (填“偏高”、“偏低”或“无影响”)。
④若滴定前以仰视的姿势读取了碱式滴定管的读数,滴定后读数正确,则测得样品中氮的质量分数________ (填“偏高”、“偏低”或“无影响”)。
⑤滴定时边滴边摇动锥形瓶,眼睛应观察______。
A.滴定管内液面的变化
B.锥形瓶内溶液颜色的变化
⑥滴定达到终点时,酚酞指示剂由______色变成________色。
(2)滴定结果如下表所示:
| 滴定次数 |
待测溶液的体积/mL |
标准溶液的体积 |
|
| 滴定前刻度/mL |
滴定后刻度/mL |
||
| 1 |
25.00 |
1.02 |
21.03 |
| 2 |
25.00 |
2.00 |
21.99 |
| 3 |
25.00 |
0.20 |
20.20 |
若NaOH标准溶液的浓度为0.10 mol/L,则该样品中氮的质量分数为________。
工业上用“三氯氢硅还原法”制备纯硅的工业流程如图: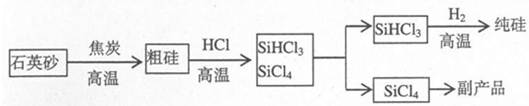
(1)石英砂的主要成分是(填化学式),在制备粗硅时焦炭的作用是。
(2)制备三氯氢硅的反应:
Si(s)+3HCl(g) SiHCl3(g)+H2(g)
SiHCl3(g)+H2(g) 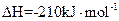
伴随的副反应为:
Si(s)+4HCl(g)  SiCl4(g)+2H2(g)
SiCl4(g)+2H2(g) 
已知SiHCl3和SiCl4常温下均为液体,工业上分离SiHCl3和SiCl4的操作方法
为;
写出SiHCl3(g)和HCl反应生成SiCl4(g)和H2的热化学方程式。
(3)该生产工艺中可以循环使用的物质是。
(4)实验室用SiHCl3与过量H2反应制备纯硅的装置如下图(热源及夹持装置略去).已知SiHCl3能与H2O强烈反应,在空气中易自燃。
①装置B中的试剂是(填名称),装置C中的烧瓶需要加热,其目的是。
②实验中先让稀硫酸与锌粒反应一段时间后,再加热C、D装置的理由是,装置D中发生反应的化学方程式为。